-
骨髓纤维化分为原发性骨髓纤维化和继发性骨髓纤维化,其中以继发性骨髓纤维化更常见。导致继发性骨髓纤维化的病因多种多样,血液系统疾病则是其主要病因之一,诸如:白血病、淋巴瘤、多发性骨髓瘤等[1]。肥大细胞增生症虽然是血液系统疾病,并且也可导致继发性骨髓纤维化,但临床极为罕见,笔者拟通过该病例及相关文献学习加深对肥大细胞增生症伴继发性骨髓纤维化的认识。
-
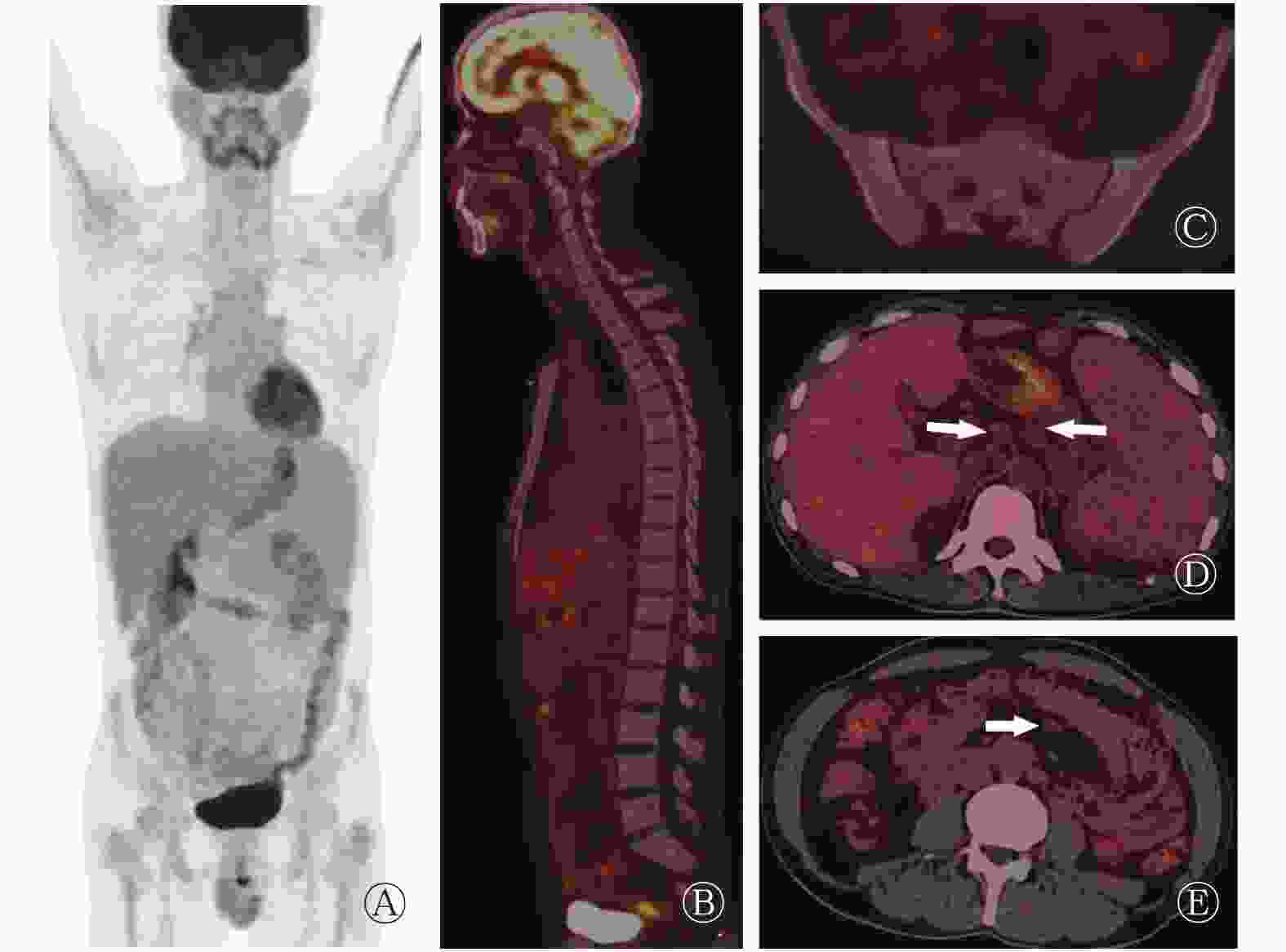
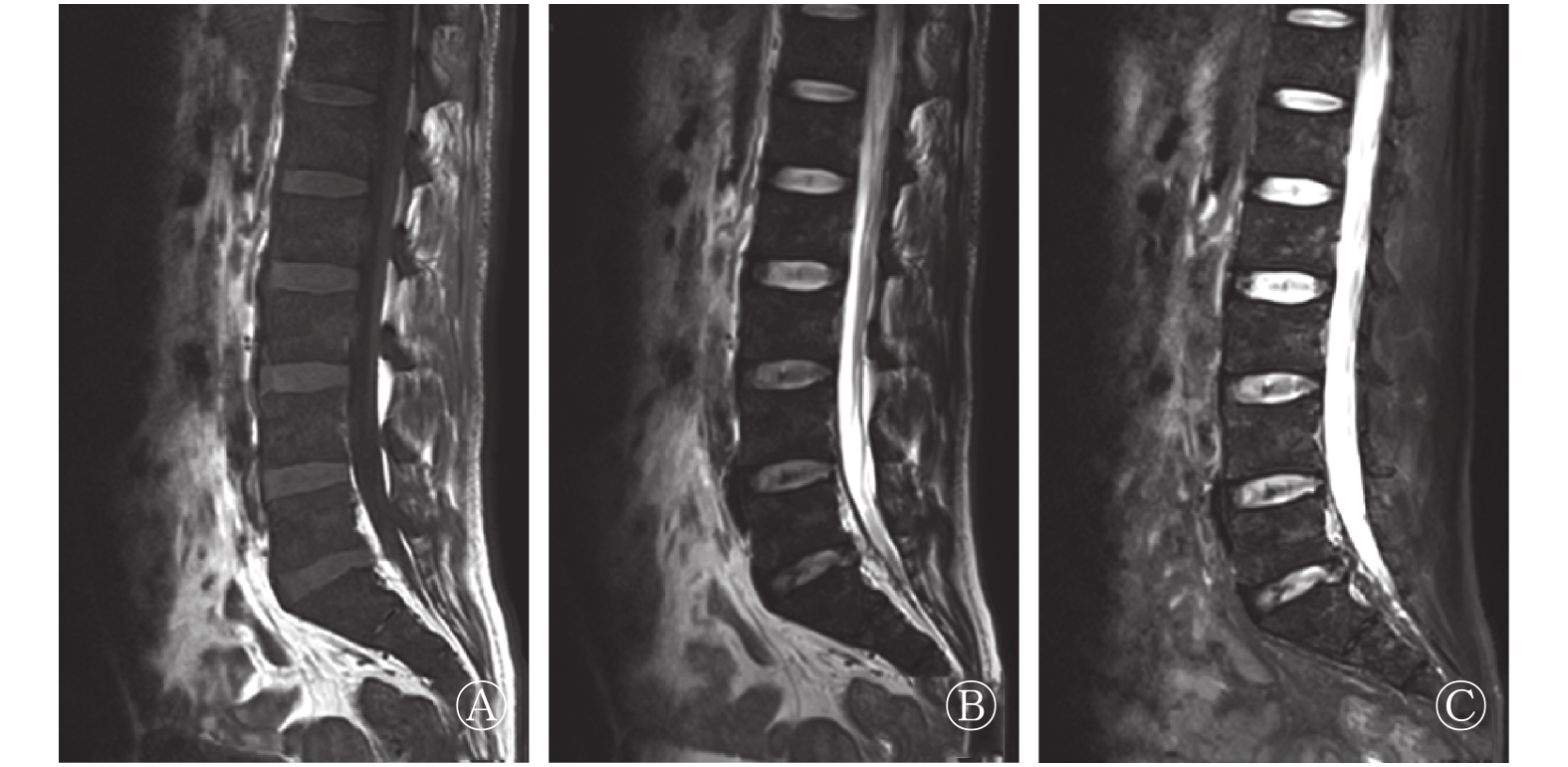
患者男性,43岁,因“活动后胸闷不适伴频发心跳加速、面部潮红,严重时甚至有濒死感”一周后入院。血液学指标:红细胞为2.66×1012个/L(正常值4.3×1012~5.8×1012个/L),白细胞为1.04×109个/L(正常值3.5×109~9.5×109个/L),血小板为151×109个/L(正常值125×109~350×109个/L)。骨髓穿刺结果提示三系增生,粒细胞、巨核细胞成熟障碍,嗜碱性粒细胞比例偏高,增生性贫血。心电图、心脏彩超、冠状动脉CT血管造影、肺功能、脑电图、脑脊液、脑部MRI均提示阴性。腰椎MRI检查(T1加权像、T2加权像及T2加权像抑脂)提示腰骶椎诸椎体信号弥漫性减低(图1中A~C)。18F-FDG PET/CT检查提示全身骨质密度弥漫性增高,代谢不高;肝脏、脾脏、腹膜后及肠系膜区多发淋巴结肿大,代谢不高(图2);18F-FDG PET/CT诊断考虑:骨髓纤维化。为进一步明确骨髓纤维化的原因,该患者再次进行了骨髓穿刺检查,最终确诊为肥大细胞增生症伴继发性骨髓纤维化。随后患者行抗组胺药物治疗,胸闷、心跳加速、面部潮红及濒死感等症状明显好转,未再发作。
-
骨髓纤维化是指骨髓造血组织被纤维组织所代替,以致影响造血功能所产生的病理状态。按病因可分为原发性骨髓纤维化和继发性骨髓纤维化,其中以继发性骨髓纤维化更为常见。原发性骨髓纤维化是起源于单个多能造血干细胞的克隆性血液病,骨髓成纤维细胞的异常增生是对造血细胞克隆性增生的继发性反应[1]。而继发性骨髓纤维化指由于各种不同病因(血液系统疾病、骨髓转移瘤、感染、代谢性疾病、免疫性疾病等)引起的骨髓中纤维组织增生[2-5],是影响造血功能的一种疾病,肥大细胞增生症便是继发性骨髓纤维化的病因之一。另外,骨髓纤维化常伴有不同程度的髓外造血(也称髓样化生),从而表现为不同程度的肝脏、脾脏及多发淋巴结肿大[1]。
肥大细胞增生症是一种皮肤、骨骼、淋巴结、内脏及单核-巨噬细胞系统中以肥大细胞异常增生为特征的极为罕见的血液系统疾病。根据肥大细胞浸润部位与程度的不同,肥大细胞增生症可分为皮肤肥大细胞增生症和系统性肥大细胞增生症两大类。皮肤肥大细胞增生症是肥大细胞增生症中最常见的类型,好发于儿童,其特征是肥大细胞仅累及皮肤,临床上表现为局部或弥漫的皮肤色素沉着,皮肤活检时真皮内有大量肥大细胞存在。系统性肥大细胞增生症是一种以多组织或器官肥大细胞异常增生为特征的疾病,好发于成年人,骨髓、肝脏、脾脏、淋巴结等组织或器官是其常见受累部位,其中以骨髓浸润最为常见,几乎所有系统性肥大细胞增生症患者均会出现肥大细胞骨髓浸润,因此骨髓穿刺是确诊系统性肥大细胞增生症至关重要的检查方法[6]。
系统性肥大细胞增生症的临床症状与肥大细胞分泌的诸多化学介质(如组胺、肝素、前列腺素、蛋白酶、肿瘤坏死因子等)密切相关,其中以组胺含量最高。因此,系统性肥大细胞增生症患者常可出现阵发性皮肤潮红、瘙痒、心悸、恶心、呕吐、腹痛、腹泻、头痛、晕厥、低血压等症状[7]。
骨质密度改变、肝脏、脾脏及淋巴结肿大是系统性肥大细胞增生症最为典型的CT表现。该类患者可出现骨质密度减低甚至骨质疏松,也可出现骨质硬化。肥大细胞分泌的肝素、前列腺素可促进骨质吸收,蛋白酶具有降解骨基质的作用,从而导致骨质密度减低甚至骨质疏松;而肥大细胞分泌的组胺则具有促进成纤维细胞活化的能力,从而促进骨质硬化甚至骨髓纤维化的形成。肝脏、脾脏及淋巴结肿大一方面是因为肥大细胞的浸润,另一方面与继发性的髓外造血有一定关系。虽然系统性肥大细胞增生症常表现为多组织器官的肥大细胞浸润,但在18F-FDG PET/CT上受累组织器官代谢并不高,具体原因尚不清楚[8-9]。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 陈建普负责论文的设计与撰写;田月丽、李崇佼负责的论文初步审阅;幸奠奎负责资料的收集;文兵、何勇负责论文的审阅及最终版本修订。
系统性肥大细胞增生症致继发性骨髓纤维化PET/CT显像一例
Myelofibrosis secondary to systemic mastocytosis: a case report of PET/CT
-
摘要: 笔者报道了一例系统性肥大细胞增生症伴继发性骨髓纤维化的18F-FDG PET/CT显像病例。从临床症状、实验室检查、影像学检查以及骨髓穿刺等结果综合分析了该病的特点。并通过文献复习加深了对骨髓纤维化及肥大细胞增生症的认识。继发性骨髓纤维化的病因多种多样,肥大细胞增生症就是其病因之一。肥大细胞增生症是一种以肥大细胞多组织器官异常增生为特征的血液系统疾病,肥大细胞分泌的组胺会导致骨质密度弥漫性增高,肝脾淋巴结肿大一方面是因为肥大细胞的浸润,另一方面则是因为髓外造血所致。另外,此类患者出现的诸多临床症状也与肥大细胞分泌的化学介质密切相关。Abstract: A case of myelofibrosis secondary to systemic mastocytosis of 18F-FDG PET/CT imaging was reported. The characteristics of the disease were analyzed on the basis of clinical symptoms, laboratory examinations, imaging examinations, and bone trephine. The understanding of myelofibrosis and mastocytosis was deepened by literature review. Secondary myelofibrosis has numerous causes, one of which is mastocytosis. Mastocytosis is a blood system disease characterized by abnormal proliferation of mast cells in multiple tissues and organs. The histamine secreted by mast cells plays an important role in osteosclerosis. Lymphadenopathy characterized by enlarged liver and spleen is due to mast cell infiltration and extramedullary hematopoiesis. Symptoms of patients are also closely related to the chemical mediators secreted by mast cells.
-
Key words:
-
-
[1] 徐海萍, 高继勇, 宋凤娟, 等. 骨髓纤维化74例临床分析[J]. 白血病·淋巴瘤, 2006, 15(5): 369−371. DOI: 10.3760/cma.j.issn.1009−9921.2006.05.018.
Xu HP, Gao JY, Song FJ, et al. Clinical analysis of 74 cases of myelofibrosis[J]. J Leuk Lymphoma, 2006, 15(5): 369−371. DOI: 10.3760/cma.j.issn.1009−9921.2006.05.018.[2] Balkan C, Ersoy B, Nese N. Myelofibrosis associated with severe vitamin D deficiency rickets[J]. J Int Med Res, 2005, 33(3): 356−359. DOI: 10.1177/147323000503300311. [3] Butt YM, Chen WN. Myelofibrosis secondary to renal osteodystrophy[J]. Blood, 2016, 128(16): 2104. DOI: 10.1182/blood−2016−07−726182. [4] Lim DJ, Oh EJ, Park CW, et al. Pancytopenia and secondary myelofibrosis could be induced by primary hyperparathyroidism[J]. Int J Lab Hematol, 2007, 29(6): 464−468. DOI: 10.1111/j.1365−2257.2006.00877.x. [5] Del Porto F, Tatarelli C, Di Napoli A, et al. Systemic lupus erythematosus and myelofibrosis: a case report and revision of literature[J]. Leuk Res Rep, 2018, 9: 58−64. DOI: 10.1016/j.lrr.2018.04.004. [6] Valent P, Horny HP, Escribano L, et al. Diagnostic criteria and classification of mastocytosis: a consensus proposal[J]. Leuk Res, 2001, 25(7): 603−625. DOI: 10.1016/S0145−2126(01)00038−8. [7] Ozdemir D, Dagdelen S, Erbas T. Systemic mastocytosis[J]. Am J Med Sci, 2011, 342(5): 409−415. DOI: 10.1097/MAJ.0b013e3182121131. [8] Fritz J, Fishman EK, Carrino JA, et al. Advanced imaging of skeletal manifestations of systemic mastocytosis[J]. Skeletal Radiol, 2012, 41(8): 887−897. DOI: 10.1007/s00256−012−1374−9. [9] Djelbani-Ahmed S, Chandesris MO, Mekinian A, et al. FDG-PET/CT findings in systemic mastocytosis: a French multicentre study[J]. Eur J Nucl Med Mol Imaging, 2015, 42(13): 2013−2020. DOI: 10.1007/s00259−015−3117−3. -






 下载:
下载: