-
【病例一】
1 简要病史与相关检查
患者男性,76岁,主诉餐后腹胀、胀气、大便干燥1月余,伴夜间盗汗、体重下降、纳差,偶尔面色潮红;就诊前4日午后及晚间低热;无咳嗽。体格检查:右下腹有触痛。实验室检查:肿瘤标志物糖类抗原724(CA724)为 7.01 U/mL(0~6.9 U/mL),总前列腺特异抗原(t-PSA)为4.285 μg/mL(0~4.0 μg/mL),癌胚抗原(CEA)、甲胎蛋白(AFP)、糖类抗原19-9(CA19-9)、细胞角蛋白19片段(Cyfra21-1)均为阴性。影像学检查:外院腹部增强CT提示腹膜、腹膜后多发结节,首先考虑转移;回盲部增厚,建议结合肠镜检查。外院胸部CT提示考虑为双肺继发性肺结核。
2 PET/CT影像学表现
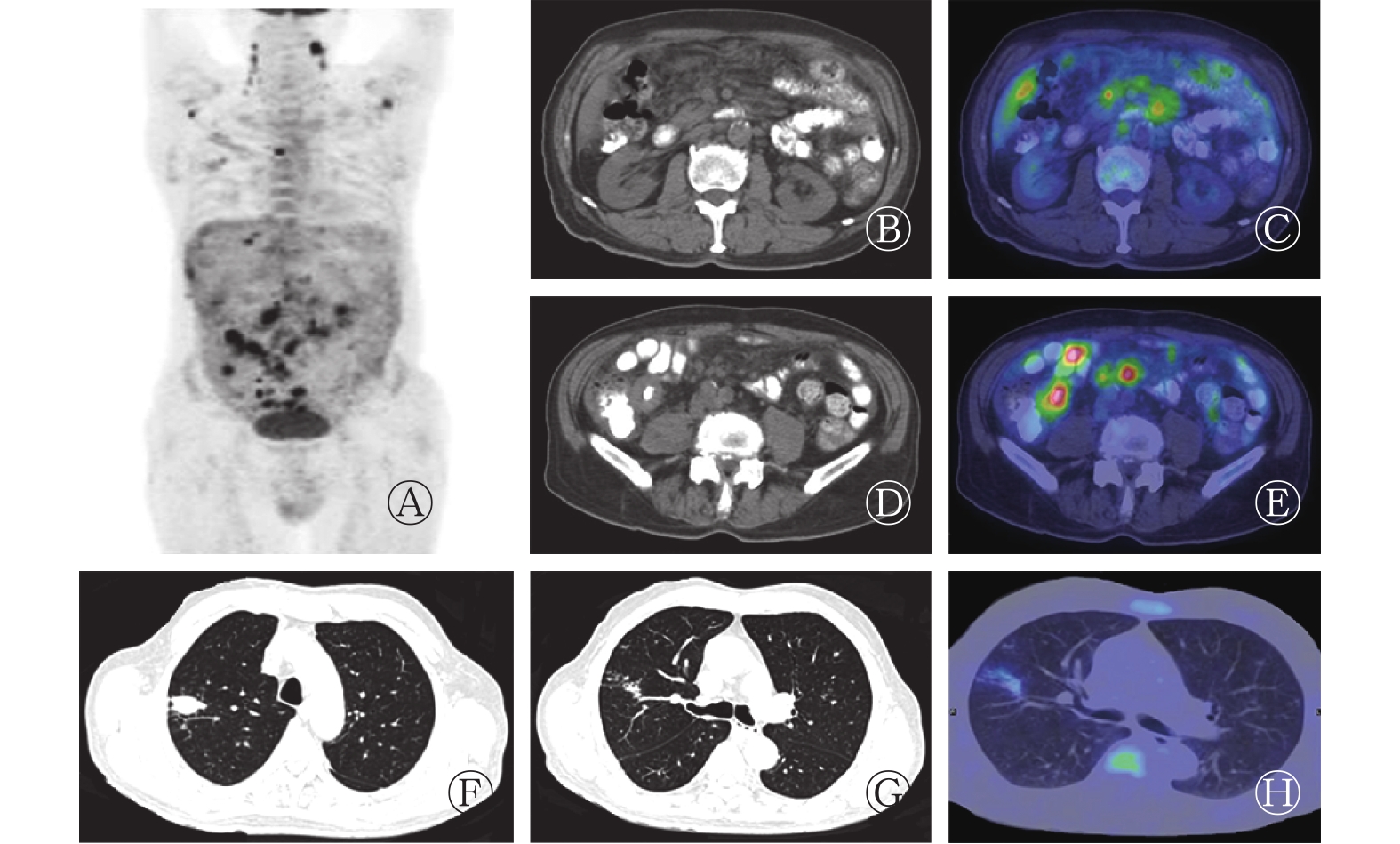
由图1可见:①右侧中下腹相当回盲区小肠多发局段肠壁增厚,CT值为56 Hu,PET显像可见明显放射性异常,SUVmax为7.8;②腹腔脂肪层混浊,肝包膜、大网膜、腹盆腔腹膜及肠系膜呈不同程度增厚,PET显像均可见放射性异常,SUVmax为7.4;③双肺多发小斑片伴小结节影,PET显像部分略见放射性异常,SUVmax为2.6;④肠系膜间及根部、腹膜后腹主动脉及下腔静脉周围、双肾血管周围、髂总动脉周围、腰大肌内侧多发结节,CT值为38 Hu,边界不清,PET显像可见放射性异常,SUVmax为9.8,病灶大者约为1.8 cm×0.8 cm。

图 1 肠结核病患者(男性,76岁)的18F-FDG PET/CT图
Figure 1. 18F-FDG PET/CT images of intestinal tuberculosis (male, 76 years old)
【病例二】
1 简要病史与相关检查
患者女性,46岁,因精神分裂症常年于安定医院住院,就诊前一周出现左髂部肿胀伴压痛。实验室检查:中性粒细胞绝对值为6.43×109/L(1.80×109/L~6.30×109/L),中性粒细胞百分比为75.9%(40.0%~75.0%),单核细胞绝对值为0.71×109/L(0.1×109/L~0.6×109/L),淋巴细胞百分比为14.4%(20.0%~50.0%)。影像学检查:外院超声示左髂骨前方囊实性肿物;外院CT提示左髂骨骨质破坏伴软组织肿物及囊变。
2 PET/CT影像学表现
由图2可见:①左侧髂窝不规则囊实性肿物,CT值为14~33 Hu,边界欠清,实性部分PET显像可见异常放射性异常,SUVmax为19.1,大小约为11.1 cm×6.9 cm,肿物与邻近髂肌分界不清,邻近左侧髂骨骨质破坏;②左侧腰大肌内侧、骶前、髂脉区、臀中-小肌间及腹股沟区多发结节,CT值为41 Hu,边界欠清,PET显像可见放射性异常,SUVmax为14.7,病灶大者约为2.4 cm×1.4 cm;③纵隔内多发结节,CT值为31 Hu,边界欠清,PET显像可见放射性异常,SUVmax为11.3,病灶大者约为1.9 cm×1.3 cm。

图 2 骨结核病患者(女性,46岁)的18F-FDG PET/CT图
Figure 2. 18F-FDG PET/CT images of bone tuberculosis (female,46 years old)
【病例三】
1 简要病史与相关检查
患者男性,61岁,6个月前因脑梗入院,外院行胸部X射线检查偶然发现肺结节,就诊2周前于外院复查胸CT提示结节较之前增大,无咳嗽、咳痰、发热、胸痛、胸闷等症状。
2 PET/CT影像学表现
由图3可见:①左肺上叶舌段结节,CT值为18 Hu,边界尚清,边缘不规整,可见多发条索,牵拉邻近胸膜,边缘可见小空泡,增强后呈不均匀强化,CT值为26~60 Hu,PET显像略见放射性异常,SUVmax为1.9,大小约为2.6 cm×1.0 cm×2.5 cm;②双侧颈血管间隙、左侧颈深、纵隔内腔静脉后、隆突下及奇食窝多发结节,CT值为36 Hu,边界清晰,增强后可见明显强化,CT值为86 Hu,PET显像未见放射性异常,病灶大者短径约为0.6 cm;③双肺多发磨玻璃影,边界尚清,PET显像未见放射性异常,大者约为0.9 cm×0.7 cm;④右侧肾上腺外侧肢及左侧肾上腺分歧部可见多发结节,CT值为33 Hu,边界尚清,增强后可见明显强化,CT值为104 Hu,PET显像可见放射性异常,SUVmax为5.9,病灶大者位于右侧肾上腺,约为1.7 cm×1.2 cm。
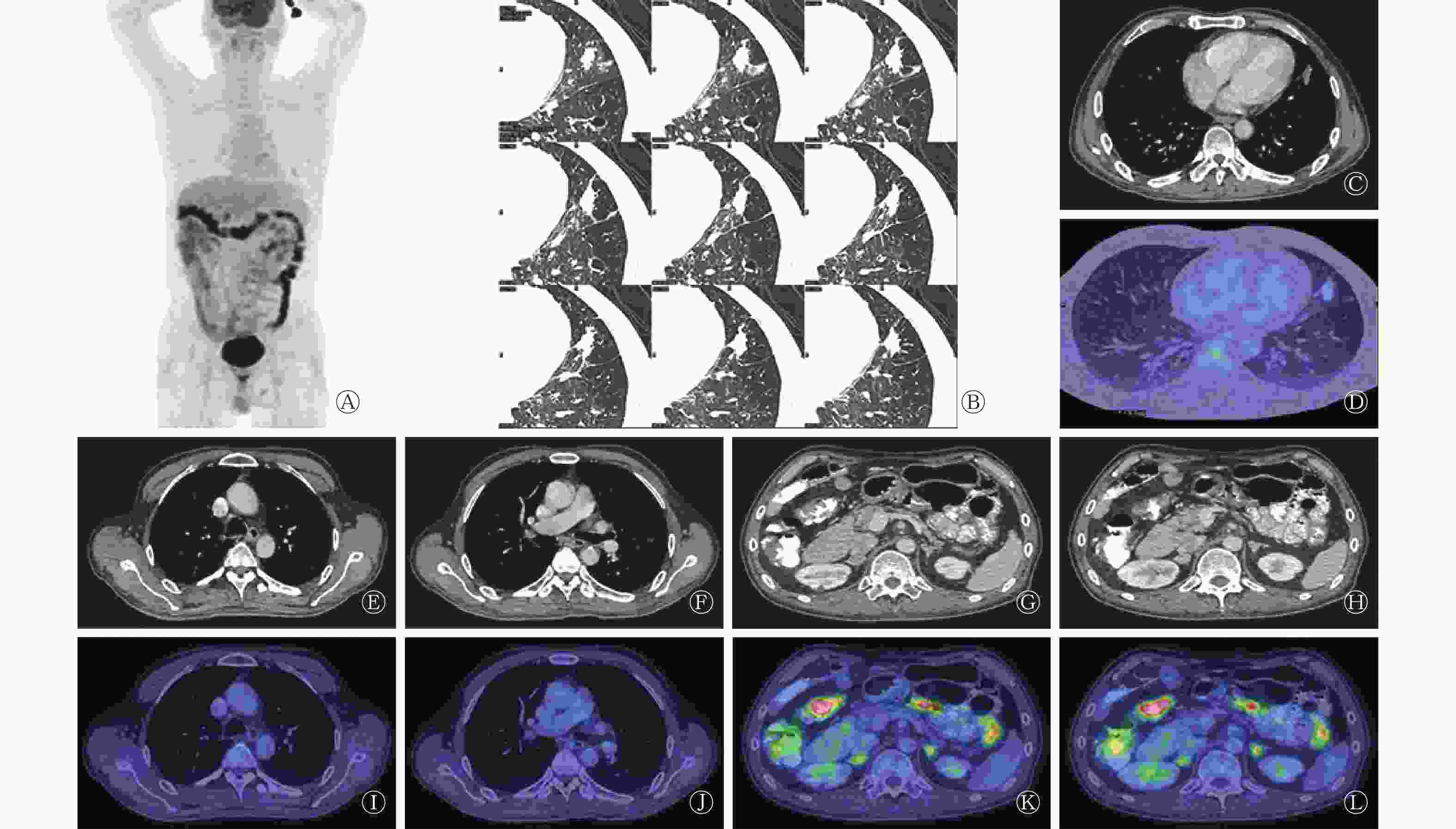
图 3 肺结核病患者(男性,61岁)的18F-FDG PET/CT图
Figure 3. 18F-FDG PET/CT images of pulmonary tuberculosis (male, 61 years old)
【影像学诊断】
病例一:恶性,淋巴瘤可能性大,不排除结核性病变。
病例二: 左侧髂窝不规则囊实性肿物伴左侧髂骨破坏,考虑为恶性可能性大,伴全身淋巴结转移,需结合活检。
病例三:左肺上叶舌段结节,考虑为周围型肺癌可能性大,右侧肾上腺外侧肢及左侧肾上腺分歧部多发结节,不排除恶性。
【病理诊断】
病例一:(回盲部)肉芽肿性炎症,伴黏膜糜烂,首先考虑结核,需结合临床及肺部检查,建议抗结核治疗后复查。
病例二:(左髂骨针吸活检)考虑肉芽肿性病变伴坏死,结核病可能性大,结合临床及相关实验室检查。
病例三:(左上肺)支气管扩张伴局灶肉芽肿性病变,结核待排除,结合临床相关检查,区域淋巴结呈反应性增生:5区1枚、6区1枚、7区2枚、10区1枚、11区3枚、12区1枚。
【讨论辨析】
结核病由结核杆菌引起,好发于青年,绝大部分发生在肺部,全身其他部位亦可继发感染。结核病患者的实验室检查结果为血沉普遍加快,肺结核病患者的痰涂片可检出结核菌,结核菌素试验结果呈强阳性是有活动性结核的依据。结核病的临床表现多种多样,活动期全身症状可有午后低热、全身乏力、消瘦、夜间盗汗等,女性可月经不调或闭经。以不同部位而言,肺结核以咳嗽、咳痰、咯血为主,多为干咳,痰液一般为白色黏痰,咯血轻者痰中带血,重者可有量不等的咯血甚至致死性的大咯血,痊愈后可反复。此外,肺结核病患者还可出现胸痛、呼吸困难、类似风湿热的结核性变态反应等非特异性的临床症状。骨结核病好发于青壮年,腰椎最常见,起病较缓慢,可有低热、盗汗、倦怠、消瘦和食欲减退等;病变部位可出现功能障碍、肿胀、疼痛、畸形等症状。肠结核病好发于回盲部,多数起病缓慢且病程长,有腹泻或便秘、腹痛、腹部包块等症状,也可只表现为右下腹以及脐周的压痛。
肠结核病主要分布于回盲部,增厚的肠壁内伴有钙化是CT图像特征性改变。CT多表现为肠壁环形增厚,边缘模糊,少数可见盲肠内侧偏心性增厚、 回盲瓣增厚,可呈肠道造影跳跃征,增强后肠壁明显强化。偶尔可见不规则混合性密度增厚伴肠腔内多个息肉样突起,增强后呈不均匀强化。PET显像中多节段增厚肠管可见弥漫性放射性异常,以溃疡为形态学基础的肠壁环形增厚则表现为异常浓聚范围小于增厚肠壁,以增生为主的肠壁偏心性增厚,与恶性肿瘤异常浓聚的方式相似,表现为肠壁结节样放射性异常[1]。病例一为老年男性患者,因餐后腹胀、大便干燥就诊,CT检查显示右侧中下腹相当回盲区小肠呈多发局段肠壁增厚,腹腔多发淋巴结肿大,脂肪层浑浊、增厚,PET显像均可见放射性异常。结合患者的发病年龄、临床症状及影像学特征应该不难想到肠癌、恶性淋巴瘤与结核的鉴别诊断。再结合实验室检查继续分析,总前列腺特异性抗原(t-PSA)升高仅与前列腺疾病有关,对本病例无临床意义;糖类抗原724(CA724)对胃癌、卵巢黏液性囊腺癌和非小细胞肺癌的诊断灵敏度较高,对结直肠癌及其他恶性肿瘤的诊断灵敏度相对较低,且该患者的CA724水平略高于正常值上限,因此肿瘤标志物检查对该患者的诊断价值不大。根据影像学特征,该患者CT影像示回盲部小肠壁增厚的形态较对称、均匀,与肠癌多表现为偏心性、非对称性肠壁增厚不一致[2],且管腔内未见明显狭窄、梗阻的征象,另外转移性淋巴结常表现为淋巴门结构消失,长短径比例失衡,也与该例患者的表现不符,据此基本可以排除肠癌。恶性淋巴瘤可以有发热、盗汗、体重下降等症状,与结核的临床表现相似,且结核与恶性淋巴瘤CT检查均可以出现肠壁环形增厚、淋巴结肿大[2],PET显像均可呈现明显的结节状放射性异常,这进一步加大了诊断的难度。但恶性淋巴瘤肠壁多为不规则增厚,黏膜增粗、变平,管壁僵硬[2],受累淋巴结无坏死,而病例一患者的CT影像显示肠壁增厚及淋巴结增大表现与此不符,且PET显像中回盲部病灶呈局灶性异常浓聚,范围略小于增厚肠壁范围,与肠结核的PET/CT影像学表现相符,因此病例一患者应首先考虑为肠结核。
骨结核病常见于腰椎,CT影像中多表现为椎体前中部为主的骨质破坏,内见多发砂粒状死骨,椎旁软组织肿胀,冷脓肿形成,冷脓肿内可见钙化[3]。结核骨质破坏区及周围软组织肿块、冷脓肿的PET/CT显像中表现为结节状、团片状及环状放射性摄取。病例二患者为中年女性患者,左髂部肿胀伴压痛就诊, CT影像示左侧髂骨骨质破坏,左侧髂窝不规则囊实性肿物,实性部分PET显像可见异常放射性异常,全身多发淋巴结肿大,PET显像可见放射性异常,累及范围较广。病例二患者全身症状不明显,病变位于左侧髂骨,并非骨结核好发部位,而髂骨又是骨恶性肿瘤的好发部位之一,且骨质破坏、软组织肿物、18F-FDG高摄取亦是骨肿瘤的征象[4-5],这些都为诊断造成了极大的困扰。骨转移瘤主要以骨质破坏及实性软组织肿物为特征,囊变很少见,且其他部位无明显原发病灶,故病例二患者不应优先考虑骨转移。而骨原发性恶性肿瘤的CT影像上通常以骨破坏、软组织肿物及肿瘤骨形成为主要征象[4],软组织肿物较大时可出现中心小片状坏死囊变,与病例二患者髂部软组织肿物的CT表现不符。仔细观察病例二患者的CT影像发现,左髂部肿物主要为囊性,囊壁光滑、厚度较均匀,PET显像囊壁可见环形放射性异常,局部实性部分可见颗粒样致密影,实验室检查提示感染可能,这与骨结核骨质破坏、多发砂粒状死骨、冷脓肿形成的特征一致[6],提示应诊断为骨结核。
肺结核病CT影像以小叶中心性、小叶性或小叶融合性阴影、小结节、肺炎样影、空洞、球形阴影、支气管肺动脉影肿大等为主要表现。增强CT影像肺结核球多无明显强化,少数可广泛强化、边缘强化、不均匀强化或分隔状强化,并多发局限低密度区。结核病18F-FDG PET/CT显像表现多样,肺内结核病灶可有斑片样、结节样高摄取,也可无异常浓聚,纵隔淋巴结也可有异常浓聚。因单发肺结核病灶形态可类似单发肺癌结节,PET显像浓聚程度与肺癌病灶有重合,肺部肿瘤标志物水平均可升高,18F-FDG PET/CT中显像诊断肺结核常被误诊为肺癌[7]。病例三为老年男性患者,因偶然发现肺结节就诊,其提供的信息不多,CT影像显示结节位于左肺上叶舌段,并非肺结核好发部位;结节可见毛刺征且牵拉胸膜,增强后强化不均,CT增高值为8~42 Hu,颈部及纵隔多发肿大淋巴结,PET显像示肺部病灶仅略见放射性异常,淋巴结病灶无明显放射性异常。有研究结果发现肺腺癌结节及肺结核结节18F-FDG摄取程度均可较低[8],且肺部病灶形态欠规则,边缘可见毛刺及条索,强化不均,CT增高值可达40 Hu以上,这些均为恶性的征象。此外,病例三患者双侧肾上腺可见多个高代谢病灶,故极易被误诊为肺癌伴肾上腺转移。但我们应注意到,病例三患者肺结节和淋巴结18F-FDG摄取程度与肾上腺病灶18F-FDG浓聚程度不一致,SUVmax相差较大,如诊断为肺癌伴肾上腺转移与这一表现并不十分相符,即使考虑到肿瘤的异质性也不太合乎情理。仔细观察肺结节可以看到结节周围毛刺较粗长,与相邻胸膜间有条索影,与肺结核病灶因炎症反应导致临近胸膜肥厚、粘连形成的条索形态较相符;我们知道肺癌结节中的多囊样透亮影因内部部分未受累肺泡腔充气而形成,肺结核病灶因坏死多在引流支气管侧形成空泡,病例三患者肺结节病灶边缘可见细小空泡,从图像特征来看更倾向于肺结核。纵隔内部分淋巴结可见明显强化,从形态上倾向于因炎症导致的反应性增生。结核病灶分为干酪型、增生型和混合型,后2种因含有郎罕巨细胞、淋巴细胞及类上皮细胞等,葡萄糖代谢旺盛,因此病例三患者的肾上腺病灶如考虑为结核,与其PET显示有较高的放射性异常摄取程度相符。
综上所述,结核病是全身性的疾病,分布广泛,可累及多发脏器,影像学表现复杂,有文献报道结核病灶的SUVmax范围与恶性肿瘤有重合[1],延迟显像SUV增加幅度亦如此[9],且多数患者的临床症状不典型,相关肿瘤标志物也可有所升高[7],容易误诊为恶性肿瘤性病变,有时鉴别诊断的难度很大。临床工作中,我们应该仔细判读图像信息,结合临床症状及实验室检查综合分析,不断积累经验,以提高对其的诊断效能。
【专家点评】
结核病在临床上是常见疾病,以肺结核多见,但可累及全身各个器官。其临床表现各异,影像学表现复杂。结核与肿瘤等疾病18F-FDG PET/CT影像诊断与鉴别是临床工作中时常面临的难题。本文通过3个不同部位肠结核、肺结核和骨结核病例,辨析18F-FDG PET/CT影像学的表现与诊断、鉴别诊断思路,详述了结核病的临床特点、实验室检查、CT影像表现细节、18F-FDG PET/CT代谢情况及其他影像的鉴别。本文对这3个结核病列分析透彻,重点突出,对结核病影像诊断及临床医师的实际工作有很大帮助。
点评专家 赵新明教授,博士生导师。现任河北医科大学第四医院暨河北省肿瘤医院核医学科及PET/CT中心主任。兼任河北省医学会核医学会主任委员,河北省抗癌协会肿瘤核医学专业委员会主任委员,中国抗癌协会肿瘤核医学专业委员会常委,中国医学装备协会核医学装备与技术专委会常委,中华医学会核医学分会肿瘤学组副组长,中国医师协会整合医学分会整合影像专业委员会副主任委员。河北省有突出贡献的中青年专家。发表学术论文100余篇。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 卢笛负责论文的撰写与修订;刘建井负责论文的审核与校对;尹国涛、于筱舟、付蔷、朱湘负责病例与文献的收集;徐文贵负责方案的提出与设计、论文的审阅。
结核病的18F-FDG PET/CT诊断辨析
Differential diagnosis and analysis of tuberculosis by 18F-FDG PET/CT
-
摘要: 结核病可以发生于全身多个脏器,且有多种多样的影像学表现,因此结核病与其他全身性疾病(尤其是肿瘤性疾病)的鉴别较为困难。18F-FDG PET/CT在全身性疾病的诊断中有一定优势,但工作中仍需结合患者的临床表现、实验室检查、病灶的CT征象及18F-FDG浓聚程度等信息进行辨析。笔者选取了临床实践中误诊的3个病例,分别为肠结核、肺结核和骨结核,分别从临床特征及18F-FDG PET/CT影像学表现等方面进行鉴别诊断,梳理诊断思路,以期为临床诊断提供帮助。Abstract: Tuberculosis can occur in multiple organs throughout the body. It's difficult to identify tuberculosis and other systemic diseases (especially tumor diseases) because of the different imaging features. 18F-FDG PET/CT has certain advantages in the diagnosis of systemic diseases, but it still needs to be analyzed in combination with clinical manifestations, laboratory tests, CT signs of lesions and concentration of 18F-FDG. The author select three cases misdiagnosed in clinical practice, namely intestinal tuberculosis, lung tuberculosis and bone tuberculosis, and analyze the clinical features and 18F-FDG PET/CT imaging features, and comb the diagnosis ideas in order to help with clinical diagnosis.
-
Key words:
-
-
[1] 刘桂超, 高硕, 蔡莉, 等. 肺外结核39例临床表现与18F-氟脱氧葡萄糖正电子发射计算机断层成像-CT的特点分析[J]. 中华结核和呼吸杂志, 2012, 35(3): 184−188. DOI: 10.3760/cma.j.issn.1001−0939.2012.03.008.
Liu GC, Gao S, Cai L, et al. Characteristics of extrapulmonary tuberculosis in 18F-FDG PET/CT: experience from 39 cases[J]. Chin J Tubere Respir Dis, 2012, 35(3): 184−188. DOI: 10.3760/cma.j.issn.1001−0939.2012.03.008.[2] Minordi LM, Vecchioli, A, Mirk P, et al. Multidetector CT in small-bowel neoplasms[J]. Radiol Med, 2007, 112(7): 1013−1025. DOI: 10.1007/s11547−007−0202−0. [3] 曹丹庆, 蔡祖龙. 全身CT诊断学[M]北京: 人民军医出版社, 2004: 628-629.
Cao DQ, Cai ZL. Whole body CT diagnostics[M]. BeiJing: People's Military Medical Publishing House, 2004: 628-629.[4] 罗振东, 陈卫国, 贾铭, 等. 髂骨原发恶性骨肿瘤的影像学表现分析[J]. 临床放射学杂志, 2011, 30(10): 1492−1496.
Luo ZD, Chen WG, Jia M, et al. Image features of primary malignant tumor in ilium[J]. J Clin Radiol, 2011, 30(10): 1492−1496.[5] 金韬, 刘巍峰, 邓志平, 等. 骨盆原发恶性骨肿瘤366例临床分析[J]. 中国肿瘤, 2013, 22(11): 935−938. DOI: 10.11735/j.issn.1004−0242.2013.11.A021.
Jin T, Liu WF, Deng ZP, et al. Clinical analysis of 366 patients with primary bone malignancy in the pelvis[J]. China Cancer, 2013, 22(11): 935−938. DOI: 10.11735/j.issn.1004−0242.2013.11.A021.[6] 綦迎成, 刘文亚, 郭佑民. 结核病影像学诊断[M]. 北京: 人民军医出版社, 2010.
Qi YC, Liu WY, Guo YM. Imaging diagnosis of tuberculosis[M]. BeiJing: People's Military Medical Publishing House, 2010.[7] 王欣璐, 尹吉林, 张金赫, 等. 60例活动性结核正电子发射体层摄影-CT误诊为恶性肿瘤的分析[J]. 中华放射学杂志, 2013, 47(1): 34−38. DOI: 10.3760/cma.j.issn.1005−1201.2013.01.009.
Wang XL, Yin JL, Zhang JH, et al. Pitfalls of fluorodeoxyglucose positron-emission tomography-CT in tuberculosis mimicking malignancy in 60 patients[J]. Chin J Radiol, 2013, 47(1): 34−38. DOI: 10.3760/cma.j.issn.1005−1201.2013.01.009.[8] 骆柘璜, 金爱芳, 彭瑛, 等. 18F-FDG PET/CT显像在单发结核结节与临床Ⅰ期非小细胞肺癌鉴别诊断中的价值[J/OL]. 新发传染病电子杂志, 2018, 3(3): 160−163[2019−04−24]. http://d.old.wanfangdata.com.cn/Periodical/xfcrbdzzz201803011.
Luo ZH, Jin AF, Peng Y, et al. 18F-FDG PET/CT in differential diagnosis of solitary pulmonary tubercular nodule and clinical stage Ⅰ non-small cell lung cancer[J/OL]. Electro J Emerging Infect Dis, 2018, 3(3): 160−163 [2019−04−24]. http://d.old.wanfangdata.com.cn/Periodical/xfcrbdzzz201803011.[9] Chen YK, Shen YY, Kao CH. Abnormal FDG PET imaging in tuberculosis appearing like lymphoma[J]. Clin Nucl Med, 2004, 29(2): 124. DOI: 10.1097/01.rlu.0000109300.89514.35. -





 下载:
下载: