-
11C-乙酸盐作为氨基酸及甾醇合成的前体,因其代谢不受葡萄糖去磷酸化的影响,被广泛应用于多种18F-FDG显像阴性的高分化、低度恶性的肿瘤显像中,弥补了18F-FDG显像的不足[1-2],大大提高了临床诊断率,是除18F-FDG外用于肿瘤显像的一种很有潜力的新型正电子显像剂。目前,11C-乙酸盐多用于肝癌和肾癌的显像及鉴别诊断[3-4]。国内外对11C-乙酸盐的自动化合成有大量的研究,主要的合成方法包括通过自动化合成设备采用固相小柱纯化法制备以及蒸馏法制备等[5-12]。目前常规放射化学合成11C-乙酸盐的路线和方法已经很成熟,关键的问题是采用自动化模块合成后如何提高合成效率,改善合成条件的方法主要有两种:缩短合成时间、在靶出口捕获氮氧化物等。本研究采用LOOP环液相法合成11C-乙酸盐,采用固相小柱水解纯化法纯化,在国产模块上进行11C-乙酸盐的自动化合成。对11C-乙酸盐的自动化合成条件进行详细研究后,得到最优化条件,以提高其合成效率,推广其临床应用。
-
Sumitomo HM-10加速器:日本住友重机械工业株式会社;PET-CS-Ⅱ-IT-I型11C-CH3I合成模块、PET-CS-I型11C-多功能合成模块:北京派特生物技术有限公司;CRC-15R活度计、Radio-TLC(放射性薄层扫描仪)、FC3200型放射性在线检测器:美国Bioscan公司;Bioscan Min-Scan扫描软件:美国Alltech公司;硅胶板:美国Whatman公司。
-
五氧化二磷柱、ICH-Ag柱、IC-OH柱、1 mol/L柠檬酸钠、0.8 mm×1.6 mm四氟管、0.8 mm×2.4 mm硅胶管:北京派特生物技术有限公司;无水四氢呋喃(tetrahydrofuran,THF):美国Adrich公司;氢氧化钠:分析纯,天津市化学试剂三厂;0.9、1.5、3.0 mol/L CH3MgBr/THF:武汉远城科技发展有限公司;冰乙酸:郑州市恩都化工有限公司;37%盐酸:镇江市化学试剂厂。
-
Sumitomo HM-10加速器质子轰击氮氧混合气,利用14N(p,α)11C核反应靶内产生11CO2。轰击能量为10 MeV、束流30 μA、轰击时间30 min。靶内生产的11CO2经释放进入合成箱,11CO2进入不锈钢捕获环冷却(捕获环浸泡在液氮中,11CO2变成干冰被捕获于环内)。此后移走液氮,捕获环升至室温,用3~15 ml/min的氮气将11CO2载入11C-多功能模块上装有一定量合适浓度CH3MgBr/THF的四氟管LOOP环中,使之充分反应,之后在一定压力氮气的推动下,转移至ICH-Ag柱及IC-OH柱,进行固相萃取,再分别用1 mmol/L乙酸、注射用水和生理盐水淋洗。产品经2 ml 1 mol/L盐酸酸化,通入氮气除去未反应的11CO2,柠檬酸钠中和,过无菌滤膜,即得11C-乙酸盐。
-
将一个装有定量氢氧化钠颗粒的小瓶置于活度计内,直接释放加速器靶内的11CO2至小瓶。此时活度计的示数即为加速器释放的11CO2活度。保持加速器能量10 MeV、束流30 μA,轰击时间30 min。重复测定5次,结果用均数±标准差(x±s)表示。
-
11C-乙酸盐活度直接从装有11C-乙酸盐产品瓶的活度计上读出。并由(1)式计算不校正合成效率:
$ ^{11}{\rm C}-乙酸盐合成效率(\%)= \frac{{^{11}{\rm C}-乙酸盐产品活度}}{{加速器释放的 ^{11}{\rm CO}_2 活度}} ×100\% $ -
采用放射性薄层色谱法测定11C-乙酸盐的放化纯度:支持体为硅胶板,展开剂为甲醇。用Bioscan Min-Scan软件分析计算产品的比移值(Rf)及放化纯度。
-
经过实验,加速器靶内11CO2手动释放,前1~3 s,平均速率为0.08 MPa/s;4~6 s,平均速率为0.05 MPa/s;7~12 s,平均速率为0.03 MPa/s,随后,自动释放。靶压由最初的0.8 MPa经过大约12 s的释放,降低至0.23 MPa,此时,加速器靶内大部分11CO2传输至捕获环,随后自动释放,靶压再由0.23 MPa降低至约0.05 MPa,靶内剩余11CO2依靠自身较小压力传输至捕获环,至此11CO2传靶结束,此方法可有效提高11CO2的捕获效率,捕获的11CO2约为总量的(99.3±0.2)%。
-
11CO2的释放时间对四氟管LOOP环内放射性活度的影响见表 1。经5次11CO2释放实验后,由表 1可知,11CO2的有效释放是反应顺利进行的重要因素。释放时间过短,11CO2释放不完全,参加反应的11CO2量少,放射性活度较低;释放时间过长,由于11CO2衰变快,放射性废气增多。因此,在本实验中,将11CO2释放时间由模块预设值120 s调整为140 s为宜。
11CO2释放时间(s) 120 130 140 150 160 11CO2废气量(MBq) 18.5±101.0 31.5±62.5 47.0±30.0 131.7±9.3 388.5±11.1 表 1 11CO2释放时间对四氟管LOOP环内放射性活度的影响(n=5)
Table 1. The influence of the release time of 11CO2 on the radioactive activity in the LOOP(n=5)
-
CH3MgBr/THF试剂浓度及用量对合成效率的影响见表 2。经5次11C-乙酸盐合成实验后,由表 2可以看出,采用0.9 mol/L CH3MgBr/THF前体时,由于本身CH3MgBr浓度较低,极易与空气中氧反应而失效,致使合成效率下降,即使增加其用量,也不能明显提高11C-乙酸盐的合成效率。采用3.0 mol/L CH3MgBr/THF前体时,合成失败。而采用1.5 mol/L前体时,当其用量<0.08 ml时,易与空气中水分反应导致11CO2相对过量,致使合成效率降低;但当其用量>0.2 ml后,又会因其易于结晶而使合成失败。所以,选择浓度为1.5 mol/L的CH3MgBr/THF,且其用量为0.1 ml较为适宜。本实验所用的不同浓度的CH3MgBr/THF试剂为同一个厂家同一个批次的产品。
CH3MgBr/THF用量(ml) CH3MgBr/THF浓度(mol/L) 0.9 1.5 3.0 0.20 31.0±1.7 42.5±2.5 失败 0.10 17.7±3.8 53.7±3.6 失败 0.08 9.4±1.1 36.4±2.1 失败 0.05 失败 18.3±5.7 13.6±2.9 注:表中,THF:四氢呋喃。 表 2 使用不同浓度(同一批次)及用量的CH3MgBr/ THF时11C-乙酸盐的合成效率(%,n=5)
Table 2. Different concentration and volume of THF with CH3MgBr result in different 11C-acetate yield(%, n=5)
-
本实验在11CO2释放口接一装有氢氧化钠的小瓶,将其置于活度计中,此时活度计显示的数值即为捕获环释放11CO2的量,同时调整氮气流速为15、10、8、5、3 ml/min,观察氮气流速对11CO2释放量的影响,结果见表 3。由表 3看出,氮气流速为8 ml/min时,11CO2的有效释放量最大。
氮气流速(ml/min) 15 10 8 5 3 11CO2放射性活度(×103 MBq) 9.40±0.0777 10.32±0.1443 11.29±0.0259 10.47±0.0222 7.29±0.1550 表 3 不同氮气流速对反应的影响
Table 3. The influence of different current rate of N2 on the reaction
-
本实验将初始氮气气压调整为0.14~0.16 MPa,运行气压调整为0.13~0.14 MPa较为适宜。不同气压(每个气压下实验10次)氮气对反应的影响见表 4。
氮气气压(MPa) 0.10 0.11 0.12 0.13 0.14 0.15 0.16 11C-乙酸盐合成成功率(%) 50 70 80 90 90 60 60 表 4 不同氮气气压对反应的影响(n=10)
Table 4. The influence of different N2 pressure on the reaction(n=10)
-
合成过程中少量水的参与会增加杂质11C-丙酮和11C-丁醇的产生[5, 11],影响11C-乙酸盐的合成效率,甚至导致合成失败。
-
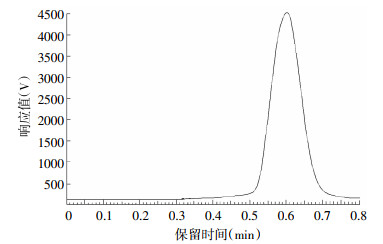
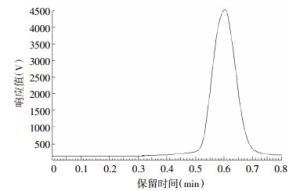
采用薄层色谱法对合成产品11C-乙酸盐进行分析,软件分析的结果见表 5,图 1为11C-乙酸盐的薄层色谱图谱。由表 5可知,11C-乙酸盐的保留时间(TR)=0.602 min,11CO2的TR=0.045 min,11C-丙酮的TR=0.150 min,由Bioscan Min-Scan软件计算得出,11C-乙酸盐的放化纯度>99%。
成份 保留时间(min) 峰面积 峰面积比例(%) 峰高(mV) 峰高比例(%) 11CO2 0.045 7429 0.03 3251 0.07 11C-丙酮 0.150 30 702 0.12 7459 0.17 11C-乙酸盐 0.602 26 469 592 99.86 4 493 345 99.76 总计 26 507 723 100 4 504 055 100 表 5 11C-乙酸盐的薄层色谱图谱分析结果
Table 5. The results of the thin layer chrommatogram on 11C-acetate
-
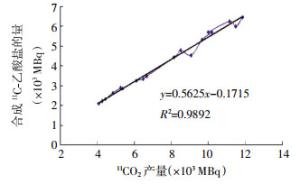
采用最佳参数(适当11CO2释放速度、140 s 11CO2释放时间、0.1 ml浓度为1.5 mol/L CH3MgBr/THF、氮气流速为8 ml/min、运行气压调整为0.13~0.14 MPa、无水条件)经18批次平行实验(同一个实验员,同一个批次试剂,相同操作,即除上述条件外其他条件均相同),11C-乙酸盐的合成效率为(53.7±3.6)%,放化纯度>99%(表 6)。其18批次平行实验的合成效率线性分析见图 2。线性相关系数R2=0.9892,高度线性相关。
11CO2产量(×103 MBq) 合成11C-乙酸盐的量(×103 MBq) 合成效率(%) 放化纯度(%) 4.070 2.087 51.3 99.2 4.255 2.213 52.0 99.3 4.440 2.313 52.1 99.5 4.847 2.623 54.1 99.6 5.254 2.893 55.1 99.6 5.365 2.853 53.2 99.2 6.105 3.252 53.3 99.1 6.475 3.334 51.5 99.2 6.660 3.482 52.3 99.6 8.140 4.436 54.5 99.7 8.510 4.777 56.1 99.5 9.065 4.540 50.1 99.8 9.657 5.321 55.1 99.6 10.180 5.702 56.0 99.8 9.990 5.705 57.1 99.2 11.140 6.249 56.1 99.3 11.470 5.998 52.3 99.6 11.840 6.453 54.5 99.4 表 6 11C-乙酸盐的合成结果分析(n=18)
Table 6. The analysis of data about synthesis of 11C-acetate(n=18)
-
因合成11C-乙酸盐的影响因素很多,初学操作合成者在常规方法下合成的成功率较低,而有经验的实验员在常规方法下合成11C-乙酸盐的产率也较低下,且质控不达标。其中对于新手来说失败的主要原因有二:①整个传输和合成通路中水分没有完全干燥,或者在用乙醇清洗LOOP环后没有用足够的氮气除去极性溶剂,而这些极性溶剂极易与格氏试剂反应,产生固态杂质阻塞管道,导致合成失败。②气态11CO2与格氏试剂一过性反应后,未反应的气态11CO2会被气体瞬间释放的压力推向废气回收管路,而在这些过程中产生巨大的阻力,易导致崩管乃至合成失败。为避免瞬间气体释放压力带来的负面影响及有助于气态11CO2与格氏试剂的充分接触,除了保证整个合成通路干净、无极性溶剂、无阻塞外,应从11CO2的传靶就开始改善常规方法。首先,不采用自动传输(即靶内的高压气体先是靠靶压将放射性11CO2气体传到合成模块上,再用高压氮气将剩余气体冲到合成模块上)[6],而是采用手动释放的方法,即手动点击靶阀,使靶内气体依靠自身压力传到捕获环上,始终控制废气量为3.7×107~7.4×107 Bq,由废气量控制手动点阀的频率及次数。其次,常规方法都采用11C-CH3I模块上预设的氮气气流大小。经试验,若预设气流过大(> 20 ml/min),11CO2气体释放的一过性压力增加过快,易导致崩管乃至合成失败;前体酸化后在ICH-Ag柱上生成絮状溴化银沉淀,使该柱阻力增加,若此时预设氮气压力较小,不足以推动2号瓶水溶液通过,从而无法到达IC-OH柱,导致合成失败。经多次尝试后,可见预设合适氮气气流大小也是至关重要的。
本研究的优化方法是针对国产模块而设计,对于国外的模块也有一定借鉴意义,因其采用的合成路线和方法都是相同的,仅是模块的设计不同而已。关于实验的重复性,不同的操作人员应用不同的国产模块采用本研究优化的条件,都应该可以减少不良因素对合成效率的影响,因为各个优化条件的操作都是有数据指标作为依据的。例如,手动传靶的操作,只要由废气量的大小来控制手动点阀的频率及次数即可。目前,国内关于11C-乙酸盐的合成研究存在的主要问题是在合成效率和质量控制方面[12],11C放射性显像剂半衰期短已经成为其发展的瓶颈,也使得11C放射性显像剂的临床应用面临两难的境地。其实,笔者认为采用自动化模块进行气液放射性化学合成本身就存在一些弊端或困难。近些年来,研究一直在关注放射性显像剂的微流体合成法[13],该方法合成时间短、效率高、选择性高、放射损失少、现用现合成。希望该新技术能够早日推广应用以改变目前临床可用放射性显像剂匮乏的现状。
自动化固相萃取法合成11C-乙酸盐的影响因素
Influential factors of solid-phase extraction method to automate the synthesis of 11C-acetate
-
摘要:
目的 探讨采用国产模块自动化固相萃取法合成11C-乙酸盐的影响因素。 方法 通过调节11C-乙酸盐合成过程中加速器靶内11CO2释放速度、捕获环释放11CO2时间、甲基溴化镁/四氢呋喃(CH3MgBr/THF)浓度及用量、氮气气流、气压及合成体系中水等参数,研究这些因素对11C-乙酸盐合成效率的影响,从而找到最优化的合成条件。 结果 经过18批次的条件优化实验后,11C-乙酸盐的合成效率为(53.7±3.6)%,放化纯度>99%。 结论 CH3MgBr/THF浓度及用量和氮气气流、气压是影响11C-乙酸盐合成效率的主要因素。 Abstract:Objective To discuss the factors that affect the synthesis of 11C-acetate via a domestic automated solid-phase extraction method. Methods The synthesis efficiency of 11C-acetate was influenced by the release rate of 11CO2 from the cyclotron target, the release time of 11CO2 by the capture ring, the concentration and volume of tetrahydrofuran(THF) with CH3MgBr, nitrogen current rate and pressure, water in the synthesis system. Thus, these parameters were optimized. Results After performing 18 runs of the conditional parallel experiment, the synthesis efficiency of 11C-acetate was increased to(53.7±3.6)%, and the radiochemical purity was more than 99%. Conclusion The main factors that affect the efficiency of 11C-acetate synthesis were the concentration and volume of CH3MgBr/THF, the current rate of nitrogen, and the pressure of nitrogen. -
Key words:
- Carbon radioisotopes /
- Acetates /
- Solid phase extraction /
- Automated synthesis /
- Influential factors
-
表 1 11CO2释放时间对四氟管LOOP环内放射性活度的影响(n=5)
Table 1. The influence of the release time of 11CO2 on the radioactive activity in the LOOP(n=5)
11CO2释放时间(s) 120 130 140 150 160 11CO2废气量(MBq) 18.5±101.0 31.5±62.5 47.0±30.0 131.7±9.3 388.5±11.1 表 2 使用不同浓度(同一批次)及用量的CH3MgBr/ THF时11C-乙酸盐的合成效率(%,n=5)
Table 2. Different concentration and volume of THF with CH3MgBr result in different 11C-acetate yield(%, n=5)
CH3MgBr/THF用量(ml) CH3MgBr/THF浓度(mol/L) 0.9 1.5 3.0 0.20 31.0±1.7 42.5±2.5 失败 0.10 17.7±3.8 53.7±3.6 失败 0.08 9.4±1.1 36.4±2.1 失败 0.05 失败 18.3±5.7 13.6±2.9 注:表中,THF:四氢呋喃。 表 3 不同氮气流速对反应的影响
Table 3. The influence of different current rate of N2 on the reaction
氮气流速(ml/min) 15 10 8 5 3 11CO2放射性活度(×103 MBq) 9.40±0.0777 10.32±0.1443 11.29±0.0259 10.47±0.0222 7.29±0.1550 表 4 不同氮气气压对反应的影响(n=10)
Table 4. The influence of different N2 pressure on the reaction(n=10)
氮气气压(MPa) 0.10 0.11 0.12 0.13 0.14 0.15 0.16 11C-乙酸盐合成成功率(%) 50 70 80 90 90 60 60 表 5 11C-乙酸盐的薄层色谱图谱分析结果
Table 5. The results of the thin layer chrommatogram on 11C-acetate
成份 保留时间(min) 峰面积 峰面积比例(%) 峰高(mV) 峰高比例(%) 11CO2 0.045 7429 0.03 3251 0.07 11C-丙酮 0.150 30 702 0.12 7459 0.17 11C-乙酸盐 0.602 26 469 592 99.86 4 493 345 99.76 总计 26 507 723 100 4 504 055 100 表 6 11C-乙酸盐的合成结果分析(n=18)
Table 6. The analysis of data about synthesis of 11C-acetate(n=18)
11CO2产量(×103 MBq) 合成11C-乙酸盐的量(×103 MBq) 合成效率(%) 放化纯度(%) 4.070 2.087 51.3 99.2 4.255 2.213 52.0 99.3 4.440 2.313 52.1 99.5 4.847 2.623 54.1 99.6 5.254 2.893 55.1 99.6 5.365 2.853 53.2 99.2 6.105 3.252 53.3 99.1 6.475 3.334 51.5 99.2 6.660 3.482 52.3 99.6 8.140 4.436 54.5 99.7 8.510 4.777 56.1 99.5 9.065 4.540 50.1 99.8 9.657 5.321 55.1 99.6 10.180 5.702 56.0 99.8 9.990 5.705 57.1 99.2 11.140 6.249 56.1 99.3 11.470 5.998 52.3 99.6 11.840 6.453 54.5 99.4 -
[1] Ho CL, Yu SC, Yeung DW. 11C-acetate PET imaging in hepatocellular carcinoma and other liver masses[J]. J Nucl Med, 2003, 44(2):213-221. [2] 霍力, 周前, 吴战宏, 等. 11C-乙酸盐PET显像在肾脏肿瘤诊断中的作用[J].中华核医学杂志, 2006, 26(4):205-208. doi: 10.3760/cma.j.issn.2095-2848.2006.04.003
[3] Mitterhauser M, Wadsak W, Krcal A, et al. New aspects on the preparation of [11C]acetate—a simple and fast approach via distillation[J]. Appl Radiat Isot, 2004, 61(6):1147-1150. doi: 10.1016/j.apradiso.2004.03.060 [4] 霍力, 周前, 傅喆. 11C-乙酸盐制备方法的改进及生物体内分布[J].国际放射医学核医学杂志, 2008, 32(4):193-196. doi: 10.3760/cma.j.issn.1673-4114.2008.04.001
[5] 张锦明, 田嘉禾, 陈燕, 等. 11C-胆碱模块合成11C-乙酸盐的研究[J].中华核医学杂志, 2008, 28(5):319-322. doi: 10.3760/cma.j.issn.2095-2848.2008.05.010
[6] Moerlein SM, Gaehle GG, Welch MJ. Robotic preparation of Sodium Acetate C 11 Injection for use in clinical PET[J]. Nucl Med Biol, 2002, 29(5):613-621. doi: 10.1016/S0969-8051(02)00307-4 [7] Soloviev D, Tamburella C. Captive solvent [11C] acetate synthesis in GMP conditions[J]. Appl Radiat Isot, 2006, 64(9):995-1000. doi: 10.1016/j.apradiso.2006.04.011 [8] Lodi F, Trespidi S, Di Pierro D, et al. A simple Tracerlab module modification for automated on-column [11C] methylation and [11C] carboxylation[J]. Appl Radiat Isot, 2007, 65(6):691-695. doi: 10.1016/j.apradiso.2006.10.011 [9] Cheung MK, Ho CL. A simple, versatile, low-cost and remotely operated apparatus for [11C] acetate, [11C]choline, [11C]methionine and [11C] PIB synthesis[J]. Appl Radiat Isot, 2009, 67(4):581-589. doi: 10.1016/j.apradiso.2008.08.018 [10] Felicini C, Nögren K, Berton A, et al. Development of an automated modular system for the synthesis of [11C] acetate[J]. Nucl Med Commun, 2010, 31(12):1033-1039. [11] Roeda D, Dollé F, Crouzel C. An improvement of 11C acetate synthesis—non-radioactive contaminants by irradiation-induced species emanating from the 11C Carbon dioxide production target[J]. Appl Radiat Isot, 2002, 57(6):857-860. doi: 10.1016/S0969-8043(02)00224-5 [12] Lodi F, Malizia C, Castellucci P, et al. Synthesis of oncological [11C] radiopharmaceuticals for clinical PET[J]. Nucl Med Biol, 2012, 39(4):447-460. [13] 金杰, 董玲, 张克华, 等.微流控合成研究进展[J].有机化学, 2012, 32(1):201-209.
-





 下载:
下载: