-
免疫球蛋白G4(Immunoglobulin G4, IgG4)相关性疾病是近几年新发现和确定的一种复合性免疫系统疾病, 其特征为血清IgG4水平升高、受累组织IgG4阳性浆细胞浸润。该病累及范围广, 包括泪腺、唾液腺、肺、胰腺、肝脏、胆管、肾脏、前列腺和后腹膜等, 临床表现为同时或不同时间各脏器肿大、结节或肥厚。因该类疾病临床症状表现各异, 临床上对此类疾病的认识尚不足, 因此, 全面、准确地诊断对患者的治疗与预后改善意义重大。
-
IgG4相关性疾病(IgG4-related disease)是近几年新发现和确认的一种可累及全身各器官、组织, 以血清IgG4水平升高、组织IgG4阳性浆细胞浸润为特征的复合性疾病, 该病病因尚不明确, 可能与遗传、感染及自身免疫等因素有关[1]。
2001年和2002年, Hamano等[2-3]关于硬化性胰腺炎患者伴有高IgG4血症且病变组织有大量IgG4阳性淋巴细胞浸润的报道开启了IgG4相关的研究之门。随后, Yamamoto等[4]研究发现米库利奇病(Mikulicz disease)患者也存在血清IgG4水平升高的现象, 从而引起日本学术界的持续关注, 为IgG4相关性疾病的发现提供了契机。2010年, IgG4相关性疾病这一新的疾病概念由日本学者在Autoimmun Rev杂志中正式提出[5]。自身免疫性胰腺炎和米库利奇病是IgG4相关性疾病最主要的病变, 此后的研究又将Riedal甲状腺炎、Kuttner肿瘤、腹膜后纤维化、炎性假瘤、间质性肾炎和间质性肺炎等均加入其中。目前证实该病可累及全身各器官及组织, 脑膜、垂体、泪腺、唾液腺、甲状腺、肺、乳腺、肝脏、胆管、胰腺、肾脏、前列腺、后腹膜、动脉、淋巴结、皮肤等均可出现该病变(表 1)[6]。
部位 病变 脑膜 硬脑膜炎 垂体 下垂体炎 泪腺 泪腺肿大、泪腺炎(Mikulicz disease) 唾液腺 肿大、唾液腺炎(Mikulicz disease)、慢性硬化性涎腺炎(Kuttner tumour) 甲状腺 慢性甲状腺炎(Riedel甲状腺炎) 肺 肺炎性假瘤、间质性肺炎 乳腺 乳腺炎性假瘤、乳腺炎 胰腺 自身免疫性胰腺炎 肝脏 肝脏炎性假瘤、肝炎 胆道 硬化性胆管炎、胆囊炎 后腹膜 腹膜后纤维化 主动脉 主动脉周纤维化 肾脏 间质性肾炎 前列腺 前列腺炎 淋巴结 淋巴结肿大 皮肤 皮肤假性淋巴瘤 表 1 IgG4相关疾病各脏器病变
Table 1. Various multi-organ manifestations in immunoglobulin G4-related disease
2011年, 日本IgG4相关性疾病研究组发布的IgG4相关性疾病诊断标准为:(1)临床表现为单一或多脏器弥漫性或特征性肿大、瘤、结节或肥厚。(2)血清IgG4水平>13.5 mg/L。(3)组织病理学表现:①有明显的淋巴细胞、浆细胞浸润及纤维化; ②IgG4阳性浆细胞浸润:IgG4/IgG阳性细胞比大于40%, 且IgG4阳性细胞超过10个/高倍视野。根据以上3个条件的符合程度, 若满足(1)+(2)+(3)可确诊, 满足(1)+(3)为拟诊, 满足(1)+(2)则为疑诊[7]。虽然IgG4相关性疾病有以上共同特征, 但由于累及器官或组织不同可出现各自差异性的表现, 给临床诊疗工作带来了挑战。作为近几年新发现和确定的一种疾病, 尚有相当一部分IgG4相关性疾病患者没有得到确诊, IgG4相关性疾病的概念、诊断及临床解析亟待重视, 为了慎重地判断多器官病变或复合性病变, 相关血液学、影像学及病理学特征、激素反应性、鉴别诊断等均应纳入临床综合考虑的范畴。
-
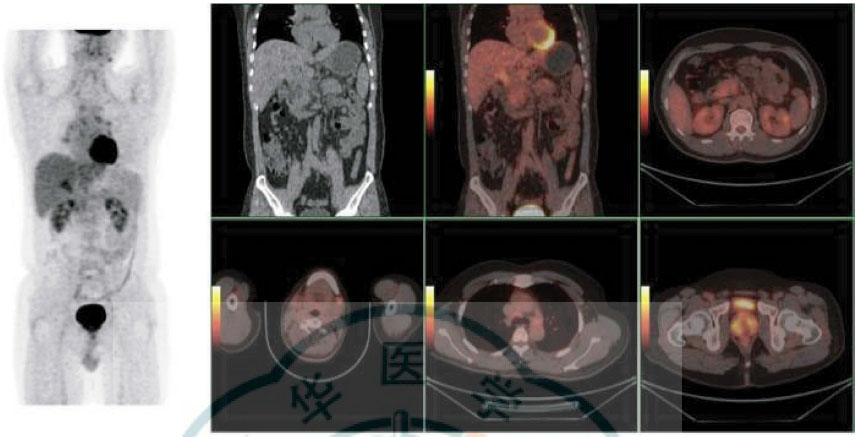
作为多模态分子影像的代表性技术, 18F-FDG PET/CT全身显像集功能成像和解剖成像于一体, 其应用贯穿于IgG4相关性疾病诊断、治疗与复发监测各环节[8]。18F-FDG PET/CT一次检查获得的全身图像可全面反映疾病累及的范围, 有利于病情评估的同时还能有效指导临床活检以便尽早确诊(图 1)。另外, 由于IgG4相关性疾病患者大部分对糖皮质激素治疗敏感, 该病仍存在一定的复发性, 因此, 18F-FDG PET/CT也成为IgG4相关性疾病的疗效评估与复发监测中不可或缺的重要手段。
-
传统影像技术反映的多为器官与组织解剖形态学变化, 18F-FDG PET/CT显像能够从分子水平反映器官与组织的功能代谢情况, 从而更早地发现IgG4相关性疾病的阳性病灶, 相对于传统CT、MRI和超声成像, 18F-FDG PET/CT对IgG4相关性疾病阳性病灶的探测具有更高的灵敏度[9]。并且, 18F-FDG PET/CT显像可一次获取患者全身图像, 能够完整地显示病灶在全身的累及部位及分布特点。既往研究报道的IgG4相关性疾病几乎可累及全身各个器官、组织, 分布主要以胰腺、泪腺和唾液腺为主, 同时或不同时间伴有其他部位自身免疫性疾病, 例如慢性甲状腺炎、硬化性胆囊炎、肺炎性假瘤、腹膜后纤维化和淋巴结肿大等[10]。IgG4相关性疾病通常具有一定的影像学特征, 主要表现为受累器官或组织弥漫性、对称性肿大或多个局灶性病灶呈散在分布等[8, 11]。再者, 通过联合所有病灶在患者全身分布的影像学特征可提高IgG4相关性疾病的诊断准确率[12]。Nakajo等[13]研究显示, 6位自身免疫性胰腺炎患者中胰腺病灶均呈18F-FDG高摄取, 其中有5位发现胰腺外18F-FDG高摄取灶:硬化性唾液腺炎(n=5)、淋巴结病(n=5)、腹膜后纤维化灶(n=2)、间质性肾炎(n=2)和硬化性胆囊炎(n=1)。因此, 18F-FDG PET/CT显像能够早期发现病变、扩大病灶视野范围, 提高疾病的检出率, 尤其对于初发症状较单一的患者, 18F-FDG PET/CT显像能获取全面的影像学信息, 从而为IgG4相关性疾病的诊断提供有力的佐证。Zhang等[14]的研究也充分肯定了18F-FDG PET/CT成像在显示IgG4相关性疾病病变特点及范围方面的作用, 并提出18F-FDG PET影像有以下5种表现的患者被诊断为IgG4相关性疾病的倾向性更高:(1)唾液腺非感染性均匀、对称性放射性摄取增高; (2)胰腺弥漫性肿大伴中-高度放射性摄取增高, 胰胆管无梗阻; (3)主动脉管壁斑片状增厚伴中-高度放射性摄取增高, 放射性摄取增高范围并不局限于血管内膜; (4)腹膜后放射性摄取中-高度增高; (5)类固醇激素治疗后2~4周病灶放射性摄取降低80%以上。
-
虽然血清IgG4水平升高是IgG4相关性疾病的一个重要特点, 但实际上血清IgG4升高还可见于过敏性皮炎、天疱疮、支气管哮喘、多中心性Castleman病和淋巴瘤等其他疾病, 此外, 约有20%~40%经活检确诊为IgG4相关性疾病的患者在诊断及激素治疗前其IgG4水平处于正常范围内, 因此临床诊疗工作中不能完全依赖IgG4的水平作为IgG4相关性疾病的诊断标准[15]。IgG4相关性疾病诊断的确立必须是要尽可能采集组织行病理学检查, 强调重视病理所见, 且一般情况下不建议激素诊断性治疗[16]。18F-FDG PET/CT显像可全面探测IgG4相关性疾病患者全身各器官系统病变, 对于18F-FDG PET/CT所显示同时存在的多器官受累, 如主动脉纤维化和颌下腺肿大, 临床可选择较表浅的颌下腺行组织病理学检查以实现早期确诊, 从而避免深部病变活检所造成的较大损伤[17-18]。因此, 18F-FDG PET/CT显像可更好地指导临床医师对IgG4相关性疾病患者行有效的病理活检, 同时尽可能地减少机体损伤, 使患者得到早期诊断和及时治疗。
-
在IgG4相关性疾病的诊断中, 自身免疫性胰腺炎(autoimmune pancreatitis, AIP)易与胰腺恶性肿瘤相混淆, 米库利奇病易与干燥综合征相混淆, 应用糖皮质激素在一定程度上可以对上述两种情况加以区别。但是, 由于激素治疗可以一定程度地改善肿瘤患者的症状, 因此激素诊断性治疗一般情况下是不推荐的[19-22]。尽管18F-FDG PET/CT显像中SUV的测定在鉴别自身免疫性胰腺炎与胰腺恶性肿瘤中的价值尚存争议[23-24], 但是18F-FDG PET/CT可同时探测到胰腺外器官受累对于提高诊断IgG4相关性疾病的信心得到了广泛认可(表 2)。Ozaki等[24]研究表明18F-FDG PET/CT有助于自身免疫性胰腺炎与胰腺癌的鉴别, 胰腺癌通常表现为胰腺结节或肿块状高代谢灶, 而自身免疫性胰腺炎多表现为胰腺长条状18F-FDG摄取增高灶, 常常伴有肺门淋巴结肿大, 其他器官如泪腺、唾液腺、胆管、腹膜后及前列腺同时受累也仅见于自身免疫性胰腺炎。不过, 也有国内研究者指出, 部分局限或多灶型的自身免疫性胰腺炎与胰腺癌的鉴别仅靠病灶形态判断仍有一定的难度, 此时观察胰管是否扩张以及胰腺外器官是否受累, 有助于自身免疫性胰腺炎的及时、准确诊断及全身评估, 同时可以提高临床医师对自身免疫性胰腺炎的认识[32]。
作者 年份 国别 研究类型 样本总数 AIP例数 AIP胰腺外受累例数 18F-FDG PET/CT显示胰腺外受累部位 Kawamura等[25] 2007 日本 回顾性 1 1 1 胆管 Ozaki等[24] 2008 日本 前瞻性 41 15 >9 泪腺、唾液腺、肺门淋巴结、胆管、腹膜后、前列腺 Sato等[26] 2008 日本 回顾性 2 2 2 下颌下腺、颈部、肺门、纵隔、腋窝及上腹部淋巴结、肢体 Matsubayashi等[31] 2009 日本 前瞻性 13 13 11 唾液腺、颈部、纵膈及腋窝淋巴结、胆管、前列腺、主动脉壁 Suga等[27] 2009 日本 回顾性 1 1 1 泪腺、下颌下腺、腹主动脉壁、腹膜后 Tomita等[28] 2010 日本 回顾性 1 1 1 泪腺、下颌下腺、胆管、腹膜后、纵膈及肺门淋巴结 Tabata等[29] 2010 日本 回顾性 1 1 1 泪腺、下颌下腺 Takahashi等[8] 2014 日本 回顾性 8 2 2 泪腺、肺门及纵膈淋巴结 Fukuhara等[30] 2014 日本 回顾性 1 1 1 肾脏 Zhang等[14] 2014 中国 前瞻性 35 18 18 唾液腺、肺、主动脉、肝脏、胆管、前列腺、多发淋巴结 Ebbo等[9] 2014 法国 回顾性 21 9 9 眼眶、腮腺、颌下腺、肺、肾脏、胆道、腹膜后、前列腺、多发淋巴结 注:表中,AIP为自身免疫性胰腺炎。 表 2 自身免疫性胰腺炎胰腺外受累:18F-FDG PET/CT价值
Table 2. Detecting extrapancreatic lesions of autoimmune pancreatitis:value of 18F-FDG PET/CT
-
目前, IgG4相关性疾病尚无统一的治疗标准, 在研究与治疗过程中发现该类患者大部分对糖皮质激素治疗反应敏感。但是, 当出现重要器官损伤或危及患者生命的严重并发症时, 需要及时采取手术及其他积极的治疗手段。有研究报道IgG4相关性疾病累及动脉血管导致动脉瘤形成[33-34], 而18F-FDG PET/CT显像可发现无明显症状的动脉受累病灶并显示其严重程度, 从而指导临床制定更科学的治疗计划, 以便早期干预阻止疾病的进程[14]。
通常情况下, 激素治疗后的观察指标是血清IgG4水平、组织器官肿胀程度以及患者临床症状改善情况, 这些受主观判断影响较大且灵敏度低。18F-FDG PET/CT显像是评估IgG4相关性疾病激素治疗效果的良好手段, 其优势在于18F-FDG PET/CT可实现治疗前后不同时间点的显像, 通过视觉及半定量分析, 了解全身病灶部位、数量和代谢程度的改变, 从而评估治疗效果、调整治疗方案及预测疾病发展趋势[8]。Ebbo等[9]对12例符合IgG4相关性疾病诊断标准的患者行18F-FDG PET显像, 发现有7例患者的18F-FDG高代谢灶在激素治疗后约5个月消失; 有2例临床及生化指标显示对治疗有一定反应性的患者病灶18F-FDG摄取与治疗前相当, 这2例患者未使用糖皮质激素、仅接受利妥昔单抗治疗; 另有2例患者治疗后病灶18F-FDG代谢进一步增高, 后被证实合并恶性淋巴瘤。Matsubayashi等[31]对11例AIP患者在糖皮质激素治疗后行18F-FDG PET显像, 患者胰腺高摄取灶大部分消失, SUVmax从5.12降至2.69, 血清IgG和IgG4水平也同时降低, 表明SUVmax与患者病情有良好的相关性, 因此, 临床可以考虑根据SUVmax的变化适当调整治疗药物的剂量。
-
尽管IgG4相关性疾病对激素治疗大多反应良好, 如:器官组织肿胀消退, 血清IgG4有所降低, 临床症状体征改善。但是长期激素治疗的不良反应多, 并且停药后IgG4相关疾病多有复发。有报道显示AIP的复发率约为10%~53%[35]。相对于传统CT、MRI、超声成像, 18F-FDG PET/CT在监测IgG4相关性疾病复发与进展方面的优势在于能够更早识别复发病灶, 尤其是在复发病灶并不仅局限于初发部位的情况下, 18F-FDG PET/CT全身显像病灶视野范围显示较广, 可实现更全面的随访监测。并且, 在临床诊疗过程中, IgG4相关性疾病合并淋巴瘤或后期并发淋巴瘤等恶性肿瘤的情况也不容忽视, 18F-FDG PET/CT在此类复杂情况下的优势地位是无可替代的[36]。
-
由于IgG4相关性疾病的认识与研究仍处于起始阶段, 多器官及组织受累交叉存在给该病的诊断造成了困难。18F-FDG PET/CT显像能够获取患者全身图像, 通过分析病灶影像学分布特征、引导临床有效活检以明确IgG4相关性疾病的诊断, 并且可实现半定量分析评估患者治疗效果、随访和监测疾病复发。有学者提出, 18F-FDG PET/CT显像应该纳入IgG4相关性疾病诊断与疗效评估标准[14]。但是, 目前有关IgG4相关性疾病18F-FDG PET/CT影像学特征与疗效评判的共识尚未达成, 治疗前后行18F-FDG PET/CT显像的最佳时间间隔的确定, 以及是否有可能通过18F-FDG PET/CT显像发现IgG4相关性疾病新的病变累及部位等也有待进一步研究。未来需要多中心、大样本的相关研究以确立18F-FDG PET/CT显像在IgG4相关性疾病诊断、治疗与随访监测中的地位。另一方面, 已有研究显示参与脱氧核苷酸补救合成的新型靶向分子探针--18F-脱氧-氟代阿糖胞苷(1-(2’-deoxy-2’-[18F] fluoroarabinofuranosyl)cytosine, FAC)在抗肿瘤免疫小鼠模型中对淋巴器官与免疫反应性病变显影良好, 18F-FAC PET/CT显像还可用于自身免疫性疾病在免疫抑制治疗后的早期疗效监测, 因此, 18F-FAC有望为IgG4相关性疾病的研究开辟新的视野[37]。毋庸置疑, PET/CT显像在IgG4相关性疾病中的广泛应用将有助于人们更全面、深入地了解这个新的疾病概念。
18F-FDG PET/CT在IgG4相关性疾病中的应用进展
The usefulness of 18F-FDG PET/CT imaging in immunoglobulin G4-related disease
-
摘要: 免疫球蛋白G4(IgG4)相关性疾病是近几年新发现和确定的一种复合性免疫系统疾病,其特征为血清IgG4水平升高、受累组织IgG4阳性浆细胞浸润。该病累及范围广,包括泪腺、唾液腺、肺、胰腺、肝脏、胆管、肾脏、前列腺和后腹膜等,临床表现为同时或不同时间各脏器肿大、结节或肥厚。全面、准确地诊断有利于该病的早期治疗和预后改善。18F-FDG PET/CT显像在IgG4相关性疾病中的诊断、疗效评估与随访监测等方面具有重要作用。笔者将对18F-FDG PET/CT在IgG4相关性疾病中的应用及研究进展进行综述。
-
关键词:
- 氟脱氧葡萄糖F18 /
- 正电子发射断层显像术 /
- 体层摄影术,X线计算机 /
- IgG4相关性疾病
Abstract: As a newly identified systemic syndrome characterized by a high level of serum immunoglobulin G4(IgG4)and dense infiltration of IgG4-positive plasma cells into multiple organs including lacrimal gland, salivary gland, lung, pancreas, liver, biliary duct, kidney, prostate, retroperitoneum and so on, IgG4-related disease(IgG4-RD)has attracted growing attention recently. Timely and accurate diagnosis is an essential prerequisite for early intervention leading to better recovery and outcome in patients with IgG4-RD. 18F-FDG PET/CT has been served as an important imaging tool for patients with IgG4-RD in assessing organ involvement, guiding biopsy and monitoring therapeutic response. This review will summarize the state-of-the-art on applications of 18F-FDG PET/CT in patients with IgG4-RD. -
表 1 IgG4相关疾病各脏器病变
Table 1. Various multi-organ manifestations in immunoglobulin G4-related disease
部位 病变 脑膜 硬脑膜炎 垂体 下垂体炎 泪腺 泪腺肿大、泪腺炎(Mikulicz disease) 唾液腺 肿大、唾液腺炎(Mikulicz disease)、慢性硬化性涎腺炎(Kuttner tumour) 甲状腺 慢性甲状腺炎(Riedel甲状腺炎) 肺 肺炎性假瘤、间质性肺炎 乳腺 乳腺炎性假瘤、乳腺炎 胰腺 自身免疫性胰腺炎 肝脏 肝脏炎性假瘤、肝炎 胆道 硬化性胆管炎、胆囊炎 后腹膜 腹膜后纤维化 主动脉 主动脉周纤维化 肾脏 间质性肾炎 前列腺 前列腺炎 淋巴结 淋巴结肿大 皮肤 皮肤假性淋巴瘤 表 2 自身免疫性胰腺炎胰腺外受累:18F-FDG PET/CT价值
Table 2. Detecting extrapancreatic lesions of autoimmune pancreatitis:value of 18F-FDG PET/CT
作者 年份 国别 研究类型 样本总数 AIP例数 AIP胰腺外受累例数 18F-FDG PET/CT显示胰腺外受累部位 Kawamura等[25] 2007 日本 回顾性 1 1 1 胆管 Ozaki等[24] 2008 日本 前瞻性 41 15 >9 泪腺、唾液腺、肺门淋巴结、胆管、腹膜后、前列腺 Sato等[26] 2008 日本 回顾性 2 2 2 下颌下腺、颈部、肺门、纵隔、腋窝及上腹部淋巴结、肢体 Matsubayashi等[31] 2009 日本 前瞻性 13 13 11 唾液腺、颈部、纵膈及腋窝淋巴结、胆管、前列腺、主动脉壁 Suga等[27] 2009 日本 回顾性 1 1 1 泪腺、下颌下腺、腹主动脉壁、腹膜后 Tomita等[28] 2010 日本 回顾性 1 1 1 泪腺、下颌下腺、胆管、腹膜后、纵膈及肺门淋巴结 Tabata等[29] 2010 日本 回顾性 1 1 1 泪腺、下颌下腺 Takahashi等[8] 2014 日本 回顾性 8 2 2 泪腺、肺门及纵膈淋巴结 Fukuhara等[30] 2014 日本 回顾性 1 1 1 肾脏 Zhang等[14] 2014 中国 前瞻性 35 18 18 唾液腺、肺、主动脉、肝脏、胆管、前列腺、多发淋巴结 Ebbo等[9] 2014 法国 回顾性 21 9 9 眼眶、腮腺、颌下腺、肺、肾脏、胆道、腹膜后、前列腺、多发淋巴结 注:表中,AIP为自身免疫性胰腺炎。 -
[1] Khosroshahi A, Stone JH. A clinical overview of IgG4-related systemic disease[J]. Curr Opin Rheumatol, 2011, 23(1):57-66. doi: 10.1097/BOR.0b013e3283418057 [2] Hamano H, Kawa S, Horiuchi A, et al. High serum IgG4 concentrations in patients with sclerosing pancreatitis[J]. N Engl J Med, 2001, 344(10):732-738. doi: 10.1056/NEJM200103083441005 [3] Hamano H, Kawa S, Ochi Y, et al. Hydronephrosis associated with retroperitoneal fibrosis and sclerosing pancreatitis[J]. Lancet, 2002, 359(9315):1403-1404. doi: 10.1016/S0140-6736(02)08359-9 [4] Yamamoto M, Ohara M, Suzuki C, et al. Elevated IgG4 concentrations in serum of patients with Mikulicz′s disease[J]. Scand J Rheumatol, 2004, 33(6):432-433. [5] Takahashi H, Yamamoto M, Suzuki CA, et al. The birthday of a new syndrome:IgG4-related diseases constitute a clinical entity[J]. Autoimmun Rev, 2010, 9(9):591-594. doi: 10.1016/j.autrev.2010.05.003 [6] Hirabayashi K, Zamboni G. IgG4-related disease[J]. Pathologica, 2012, 104(2):43-55. [7] Umehara H, Okazaki K, Masaki Y, et al. Comprehensive diagnostic criteria for IgG4-related disease(IgG4-RD), 2011[J]. Mod Rheumatol, 2012, 22(1):21-30. doi: 10.3109/s10165-011-0571-z [8] Takahashi H, Yamashita H, Morooka MA, et al. The utility of FDG-PET/CT and other imaging techniques in the evaluation of IgG4-related disease[J]. Joint Bone Spine, 2014, 81(4):331-336. doi: 10.1016/j.jbspin.2014.01.010 [9] Ebbo M, Grados A, Guedj E, et al. Usefulness of 2-18F-fluoro-2-deoxy-D-glucose-positron emission tomography/computed tomography for staging and evaluation of treatment response in IgG4-related disease:a retrospective multicenter study[J]. Arthritis Care Res(Hoboken), 2014, 66(1):86-96. doi: 10.1002/acr.22058 [10] Mahajan VS, Mattoo H, Deshpande V, et al. IgG4-Related disease[J]. Annu Rev Pathol, 2014, 9:315-347. doi: 10.1146/annurev-pathol-012513-104708 [11] Proctor RD, Rofe CJ, Bryant T, et al. Autoimmune pancreatitis:An illustrated guide to diagnosis[J]. Clin Radiol, 2013, 68(4):422-432. [12] Santhosh S, Mittal BR, Bhasin DA, et al. Role of 18F-fluorodeoxyglucose positron emission tomography/computed tomography in the characterization of pancreatic masses:Experience from tropics[J]. J Gastroenterol Hepatol, 2013, 28(2):255-261. [13] Nakajo M, Jinnouchi S, Fukukura YA, et al. The efficacy of whole-body FDG-PET or PET/CT for autoimmune pancreatitis and associa-ted extrapancreatic autoimmune lesions[J]. Eur J Nucl Med Mol Imaging, 2007, 34(12):2088-2095. doi: 10.1007/s00259-007-0562-7 [14] Zhang J, Chen H, Ma Y, et al. Characterizing IgG4-related disease with 18F-FDG PET/CT:a prospective cohort study[J]. Eur J Nucl Med Mol Imaging, 2014, 41(8):1624-1634. doi: 10.1007/s00259-014-2729-3 [15] Stone JH, Khosroshahi A, Deshpande V, et al. Recommendations for the nomenclature of IgG4-related disease and its individual organ system manifestations[J]. Arthritis Rheum, 2012, 64(10):3061-3067. doi: 10.1002/art.34593 [16] Research Committee to establish diagnostic criteria and development of treatment for systemic IgG4-related sclerosing disease; Research Committee to establish a new clinical entity, IgG4-related multi-organ lymphoproliferative syndrome(IgG 4-MOLPS). Comprehensive diagnostic criteria for IgG4-related disease(IgG4-RD), 2011. Research Program of Intractable Disease provided by the Ministry of Health, Labor, and Welfare of Japan[J]. Nihon Naika Gakkai Zasshi. 2012, 101(3):795-804. doi: 10.2169/naika.101.795 [17] Takuma K, Kamisawa T, Gopalakrishna R, et al. Strategy to differentiate autoimmune pancreatitis from pancreas cancer[J]. World J Gastroenterol, 2012, 18(10):1015-1020. doi: 10.3748/wjg.v18.i10.1015 [18] Nakatani K, Nakamoto Y, Togashi K. Utility of FDG PET/CT in IgG4-related systemic disease[J]. Clin Radiol, 2012, 67(4):297-305. [19] Matsumoto I, Shinzeki M, Toyama H, et al. A focal mass-forming autoimmune pancreatitis mimicking pancreatic cancer with obstruction of the main pancreatic duct[J]. J Gastrointest Surg, 2011, 15(12):2296-2298. doi: 10.1007/s11605-011-1543-5 [20] Himi T, Takano K, Yamamoto M, et al. A novel concept of Mikulicz′s disease as IgG4-related disease[J]. Auris Nasus Larynx, 2012, 39(1):9-17. doi: 10.1016/j.anl.2011.01.023 [21] Yao Q, Wu G, Hoschar A. IgG4-related Mikulicz′s disease is a multi-organ lymphoproliferative disease distinct from Sjogren′s syndrome:a Caucasian patient and literature review[J]. Clin Exp Rheumatol, 2013, 31(2):289-294. [22] Ketwaroo GA, Sheth S. Autoimmune pancreatitis[J]. Gastroenterol rep(Oxf), 2013, 1(1):27-32. [23] Imdahl A, Nitzsche E, Krautmann F, et al. Evaluation of positron emission tomography with 2-[18F] fluoro-2-deoxy-D-glucose for the differentiation of chronic pancreatitis and pancreatic cancer[J]. Br J Surg, 1999, 86(2):194-199. [24] Ozaki Y, Oguchi K, Hamano H, et al. Differentiation of autoimmune pancreatitis from suspected pancreatic cancer by fluorine-18 fluorodeoxyglucose positron emission tomography[J]. J Gastroenterol, 2008, 43(2):144-151. doi: 10.1007/s00535-007-2132-y [25] Kawamura E, Habu D, Higashiyama SA, et al. A case of sclerosing cholangitis with autoimmune pancreatitis evaluated by FDG-PET[J]. Ann Nucl Med, 2007, 21(4):223-228. [26] Sato M, Okumura T, Shioyama Y, et al. Extrapancreatic F-18 FDG accumulation in autoimmune pancreatitis[J]. Ann Nucl Med, 2008, 22(3):215-219. [27] Suga K, Kawakami Y, Hiyama A, et al. F-18 FDG PET-CT findings in mikulicz disease and systemic involvement of IgG4-Related lesions[J]. Clin Nucl Med, 2009, 34(3):164-167. [28] Tomita H, Matsubayashi H, Sasaki K, et al. A case of autoimmune pancreatitis accompanied with Mikulicz′s disease[J]. Nihon Shokakibyo Gakkai Zasshi. 2010, 107(5):775-783. [29] Tabata R, Tabata C, Okamoto T, et al. Autoimmune pancreatitis associated with myelodysplastic syndrome[J]. Int Arch Allergy Immunol, 2010, 151(2):168-172. [30] Fukuhara H, Taniguchi Y, Matsumoto M, et al. IgG4-related tubulointerstitial nephritis accompanied with cystic formation[J]. BMC Urol, 2014, 14:54. doi: 10.1186/1471-2490-14-54 [31] Matsubayashi H, Furukawa H, Maeda AA, et al. Usefulness of positron emission tomography in the evaluation of distribution and activity of systemic lesions associated with autoimmune pancreatitis[J]. Pancreatology, 2009, 9(5):694-699. doi: 10.1159/000199439 [32] 张建, 余仲飞, 胡胜平, 等. 18F-FDG PET/CT在自身免疫性胰腺炎诊断及全身评价中的应用.中华胰腺病杂志, 2014, 14(4):247-251. doi: 10.3760/cma.j.issn.1674-1935.2014.04.009
[33] Agaimy A, Weyand M, Strecker T. Inflammatory thoracic aortic aneurysm(lymphoplasmacytic thoracic aortitis):a 13-year-experience at a German Heart Center with emphasis on possible role of IgG4[J]. Int J Clin Exp Pathol, 2013, 6(9):1713-1722. [34] Holubec T, Laco J, Holubcova Z, et al. Repair of thoracic aortic aneurysm due to noninfectious aortitis[J]. J Card Surg, 2012, 27(2):199-204. doi: 10.1111/j.1540-8191.2011.01399.x [35] Kamisawa T, Okazaki K, Kawa SA, et al. Japanese consensus guidelines for management of autoimmune pancreatitis:Ⅲ. Treatment and prognosis of AIP[J]. J Gastroenterol, 2010, 45(5):471-477. doi: 10.1007/s00535-010-0221-9 [36] 邓雪蓉, 张卓莉. IgG4相关疾病合并淋巴瘤一例[J].中华风湿病学杂志, 2014, 18(8):574-576, 后插1. doi: 10.3760/cma.j.issn.1007-7480.2014.08.020
[37] Radu CG, Shu CJ, Nair-Gill E, et al. Molecular imaging of lymphoid organs and immune activation by positron emission tomography with a new[(18)F]-labeled 2'-deoxycytidine analog[J]. Nat Med, 2008, 14(7):783-788. doi: 10.1038/nm1724 -






 下载:
下载: