-
尼可胺是以烟酰胺为母体化合物合成的烟酰氨基酸类化合物,该化合物的肿瘤放射增敏作用显著,毒性低[1-3],很有希望成为肿瘤放疗中高效、低毒且有实用前景的放射增敏剂。为了评价尼可胺的安全性,本实验按照一类新药生殖毒性的评价要求[4-5],对尼可胺的一般生殖毒性进行了研究,以期为临床安全用药提供实验依据。
-
尼可胺由中国医学科学院放射医学研究所药物室提供,呈白色粉末状,纯度 > 98%。
-
无特定病原体级体质量为120~140 g的健康、成年Wistar大鼠购于山东鲁抗医药股份有限公司;饲养环境:屏障环境,室温控制在21~24 ℃,湿度为40%~52%,12 h照明、12 h黑暗;鼠颗粒饲料由山东大学实验动物中心提供。
-
取健康、成年雄性Wistar大鼠100只,随机分为4组,即尼可胺高剂量组(每次注射剂量为300 mg/kg)、中剂量组(每次注射剂量为200 mg/kg)、低剂量组(每次注射剂量为100 mg/kg)和空白对照组(0.9%氯化钠注射液),每组25只。雄性大鼠交配前给药5周,每天给药一次,给药体积均为1.0 ml/100 g体质量,给药持续整个交配期直至处死。给药5周后,取100只健康、成年的雌性Wistar大鼠(不做任何处理)与雄性大鼠随机1:1合笼交配,以阴栓阳性或阴道涂片精子阳性视为妊娠第0日。雄性大鼠在交配后处死,进行终末检查。
-
给药期间每天于给药前、后观察大鼠的外观体征、行为活动和死亡情况,每周测定一次摄食量和体质量。
-
处死大鼠后,分别检测各剂量组大鼠的精子活力、精子总数及精子活率。
精子活力检查:在25~28 ℃室温下,取1侧附睾头(每次取材的重量尽量保持一致),放入在37 ℃水浴中预热的装有10 ml生理盐水的平皿中,剪碎制成精子悬液。在37 ℃水浴中静置20 min后,立即吸取0.1 ml悬液滴于37 ℃预热的血细胞计数板上,在显微镜下快速观察,参照精子活力分级标准[6]:Ⅰ级为活动力良好:精子活动良好,呈直线游动;Ⅱ级为活动一般:精子活动比较活泼,但游泳方向不定,不呈直线状;Ⅲ级为活动不良:精子活动迟缓,原地打转;Ⅳ级为死精子:有精子形态,但无活动力。记录200个精子中各级活动精子的数量,计算出其百分率。
精子计数:将上述细胞计数板于4 ℃冷却后,按红细胞计数方法对所制备的精子悬液进行精子计数。
精子活率检查:取精子悬液1 ml,加0.4%台盼兰0.1 ml,在显微镜下观察,深染者为死精子,计数100个精子中活精子的比例。
-
各组动物处死后取出睾丸、附睾称湿重,并计算脏器系数。
脏器系数=器官湿重(g)/体质量(g)×100%
-
交配率=交配成功动物数/实验动物数×100%
-
将睾丸、附睾用10%中性福尔马林缓冲液固定,按常规方法进行包埋、切片、苏木精-伊红染色后,在光学显微镜下观察。
-
体质量、脏器系数、精子数等计量资料均采用x±s表示,两组间比较用t检验,P<0.05表示差异有统计学意义。
-
高剂量组:给药过程中大鼠挣扎,给药后即刻出现呼吸急促、自主活动减少等毒性反应症状;给药第8日,个别动物出现稀便、背毛竖立;给药第10日,出现稀便、背毛竖立症状的大鼠数量略有增加;给药第14日,稀便、背毛竖立症状基本消失。
中剂量组:给药过程中大鼠挣扎,给药后即刻出现呼吸急促、自主活动减少等毒性反应症状;给药第8日,个别动物出现稀便、背毛竖立;给药第10日,出现稀便、背毛竖立症状的大鼠数量略有增加;给药第13日,稀便、背毛竖立症状基本消失。
低剂量组:给药期间,大鼠一般症状观察指标均未见明显异常。
空白对照组:给药期间,大鼠一般症状观察指标均未见明显异常。
-
给药期间,尼可胺各剂量组大鼠摄食量均呈增长趋势,高、中剂量组给药第7、14、21、28、35日的摄食量几乎均低于空白对照组,且呈剂量-效应关系(随剂量升高,摄食量递减)(表 1)。
组别 大鼠数量 给药时间 7 d 14 d 21 d 28 d 35 d 髙剂量组 25 14.0a 17.6a 18.1a 20.7a 21.6a 中剂量组 25 16.7b 18.3b 19.0b 21.0b 22.5b 低剂量组 25 19.5c 19.4。 20.1。 21.5。 22.8。 空白对照组 25 19.1 18.7 18.8 21.2 22.6 注:表中,a表示与空白对照组相比,t=0.052、0.500、0.322、0.922、0.556,P>0.05;b表示与空白对照组相比,t=0.050、0.620、0.782、0.905、0.965,P>0.05;c表示与空白对照组相比,t=0.653、0.051、0.219、0.882、0.947,P>0.05。 表 1 雄性Wistar大鼠尾静脉注射不同剂量的尼可胺后摄食量的变化
(g/只/d) -
尼可胺各剂量组及空白对照组大鼠交配前随给药时间的增加,体质量均呈增长趋势,各剂量组与空白对照组相应时间点比较,体质量差异无统计学意义(表 2)。
组别 大鼠数量 给药前 给药时间 7 d 14 d 21 d 28 d 35 d 高剂量组 25 133.4±11.8a 161.3±14.4a 206.2±23.1a 235.0±28.0a 267.6±31.9a 296.9±23.9a 中剂量组 25 136.1±ll.lh 151.6±13.2h 202.7±20.6b 233.6±24.5h 260.2±28.7b 291.9±23.2b 低剂量组 25 138.4±13.1c 175.3±14.5c 210.6±17.2c 236.2±18.4c 261.4±20.7c 293.4±14.3c 空白对照组 25 130.0±12.4 175.0±17.6 210.4±20.7 236.3±26.2 270.9±29.9 300.7±22.8 注:表中,a表示与空白对照组相比,t=0.330、0.004、0.515、0.866、0.703、0.567,P>0.05;b表示与空白对照组相比,t=0.079、0.000、0.202、0.716、0.208、0.166,P>0.05;c表示与空白对照组相比,t=0.028、0.955、0.971、0.989、0.204、0.189,P>0.05。 表 2 雄性Wistar大鼠尾静脉注射不同剂量的尼可胺前后体质量变化
[(x±s)g] -
尼可胺各剂量组与空白对照组相比,大鼠精子总数、精子活力及精子活率差异无统计学意义(表 3)。
组别 大鼠数量 精子数(×103个/μl) 精子活率(%) 精子活力(%) Ⅰ级 Ⅱ级 Ⅲ级 Ⅳ级 高剂量组 25 4.3±0.6a 73.4±7.5a 4.6±2.2a 20.6±6.9a 39.4±7.2a 35.4±6.7a 中剂量组 25 4.5±0.5h 72.9±7.9b 6.5±1.8h 21.8±8.6b 33.5±9.4b 38.2±12.3b 低剂量组 25 4.2±0.5c 74.3±9.3c 5.3±2.5c 24.2±10.4c 35.6±8.5c 34.9±11.8c 空白对照组 25 4.4±0.5 73.0±12.0 5.6±3.3 26.5±10.8 34.2±10.2 34.0±16.3 注:表中,a表示与空白对照组相比,t=0.618、0.878、0.325、0.028、0.043、0.615,P>0.05;b表示与空白对照组相比,t=0.471、0.967、0.147、0.097、0.824、0.537,P>0.05;c表示与空白对照组相比,t=0.200、0.679、0.941、0.465、0.599、0.753,P>0.05。 表 3 尼可胺各剂量组雄性Wistar大鼠精子数、精子活率及精子活力的检查结果
(x±s) -
尼可胺各剂量组与空白对照组相比,大鼠生殖器官脏器系数差异无统计学意义(表 4)。
组别 大鼠数量 睾丸 附睾 高剂量组 25 0.86±0.12a 0.30±0.05a 中剂量组 25 0.88±0.12b 0.33±0.07b 低剂量组 25 0.87±0.14c 0.30±0.06c 空白对照组 25 0.84±0.15 0.29±0.05 注:表中,a表示与空白对照组相比,t=0.685、0.557,P>0.05;b表示与空白对照组相比,t= 0.379、0.489,P>0.05;c表示与空白对照组相比,t=0.489、0.477,P>0.05。 表 4 雄性Wistar大鼠尾静脉注射不同剂量的尼可胺后的脏器系数
[(x±s)%] -
尼可胺各剂量组雄性大鼠的交配率未见明显差异(表 5)。
组别 交配动物数 交配成功数 交配率(%) 高剂量组 25 20 80.0 中剂量组 25 21 84.0 低剂量组 25 20 83.3 空白对照组 25 21 87.5 表 5 雄性Wistar大鼠尾静脉注射不同剂量尼可胺后的生殖毒性实验交配率
-
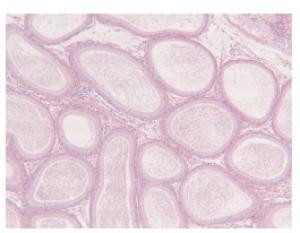
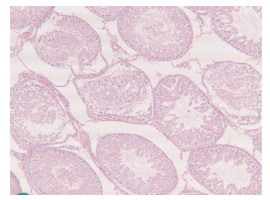
组织病理学检查发现,尼可胺为200 mg/kg及以下剂量时对成年雄性大鼠无生殖毒性作用,在300 mg/kg时对成年雄性大鼠的生殖能力有一定的影响:①睾丸:部分生精小管萎缩,精原细胞、精母细胞及支持细胞均明显脱落,精子细胞数减少(图 1)。②附睾:部分附睾管空虚,无精子或精子数减少;间质散在炎细胞浸润,以淋巴细胞为主;间质成纤维细胞增生(图 2)。
-
近年来,为了与国际接轨,我国要求必须对创新药做一般生殖毒性试验。国内相关的研究在受试药品的剂量设计、动物数量、试验指标设定、观察内容和数据统计方法等方面的差异较大[7-8]。国家食品药品监督管理局参照《药品注册的国际技术要求(安全性部分)》[9]于2006年制定了我国的《药物生殖毒性研究技术指导原则》[10],该指导原则规范了基本的试验方法。为了临床安全用药,我们按照新药审批要求,对尼可胺的一般生殖毒性进行研究,为临床应用提供理论依据。
体质量是反映动物生长发育的客观指标[11]。在本研究中,给药期间各剂量组大鼠摄食量总体呈增长趋势,体质量也呈增长趋势,与对照组比较无显著性差异,说明一定剂量的尼可胺对雄性大鼠的体质量影响不大。
睾丸和附睾的发育可反映生殖机能的发育状况,精子数量、精子活力及精子活率更是反映其生精功能的重要指标。本研究结果表明,各剂量组雄性大鼠精子数量、精子活力及精子活率各项指标与空白对照组相比无明显差异;组织病理学检查发现,尼可胺为200 mg/kg及以下剂量时,对成年雄性大鼠无生殖毒性作用,但剂量为300 mg/kg时,Wistar大鼠的睾丸、附睾有不同程度的病理改变。观察给药后的一般状况时,发现尼可胺高(300 mg/kg)、中(200 mg/kg)剂量组雄性大鼠即刻出现明显的毒性反应症状,并对给药局部血管有一定的刺激性。这些结果提示,在本实验室条件下,雄性大鼠尾静脉注射尼可胺由交配前到交配期直至胚胎着床,在200 mg/kg及以下剂量时对成年雄性大鼠无生殖毒性作用,在300 mg/kg时可能对大鼠的生殖能力有一定的影响。
放射增敏剂尼可胺对雄性大鼠生殖毒性的研究
The reproductive toxicity of NiKeAn in male rats
-
摘要:
目的 观察尼可胺对雄性大鼠生殖能力的影响。 方法 将100只健康成年雄性Wistar大鼠随机分为4组:空白对照组(0.9%氯化钠注射液)、尼可胺高剂量组(300 mg/kg)、尼克胺中剂量组(200 mg/kg)和尼克胺低剂量组(100 mg/kg)。雄性大鼠连续尾静脉注射给药5周后(每日1次),与100只雌性Wistar大鼠随机1:1合笼交配,交配后处死雄性大鼠,检查尼可胺对各剂量组雄性大鼠的交配率、精子数量、精子活率、精子活力、脏器系数的影响及睾丸、附睾的组织病理学变化。 结果 200 mg/kg以下剂量对成年雄性大鼠检测的生育指标无明显影响。 结论 200 mg/kg以下剂量对成年雄性大鼠的生殖功能无明显毒性作用。 Abstract:Objective To observe the toxic effects of NiKeAn on the ability of reproduction in male rats. Methods One hundred health adult Wistar rats were randomly divided into 4 groups with 25 in each group. The rats of control groups were given intravenous injections with normal saline and the experimental groups received NiKeAn at doses of 300 mg/kg, 200 mg/kg and 100 mg/kg once per day. All rats were injected for 5 weeks then mated and executed. The coefficient of testicle and epididymis, mating rate, sperm, the percentage of motile sperm, and histopathological changes of testicle and epididymis were detected. Results Under doses of 200 mg/kg concentration of NiKeAn used in this study have no significant influence on the aforementioned parameters. Conclusion Under doses of 200 mg/kg, reproductive function of male rats does not obviously impaired by NiKeAn. -
Key words:
- Preconception injuries /
- Rats, Wistar /
- NiKeAn
-
表 1 雄性Wistar大鼠尾静脉注射不同剂量的尼可胺后摄食量的变化
(g/只/d) 组别 大鼠数量 给药时间 7 d 14 d 21 d 28 d 35 d 髙剂量组 25 14.0a 17.6a 18.1a 20.7a 21.6a 中剂量组 25 16.7b 18.3b 19.0b 21.0b 22.5b 低剂量组 25 19.5c 19.4。 20.1。 21.5。 22.8。 空白对照组 25 19.1 18.7 18.8 21.2 22.6 注:表中,a表示与空白对照组相比,t=0.052、0.500、0.322、0.922、0.556,P>0.05;b表示与空白对照组相比,t=0.050、0.620、0.782、0.905、0.965,P>0.05;c表示与空白对照组相比,t=0.653、0.051、0.219、0.882、0.947,P>0.05。 表 2 雄性Wistar大鼠尾静脉注射不同剂量的尼可胺前后体质量变化
[(x±s)g] 组别 大鼠数量 给药前 给药时间 7 d 14 d 21 d 28 d 35 d 高剂量组 25 133.4±11.8a 161.3±14.4a 206.2±23.1a 235.0±28.0a 267.6±31.9a 296.9±23.9a 中剂量组 25 136.1±ll.lh 151.6±13.2h 202.7±20.6b 233.6±24.5h 260.2±28.7b 291.9±23.2b 低剂量组 25 138.4±13.1c 175.3±14.5c 210.6±17.2c 236.2±18.4c 261.4±20.7c 293.4±14.3c 空白对照组 25 130.0±12.4 175.0±17.6 210.4±20.7 236.3±26.2 270.9±29.9 300.7±22.8 注:表中,a表示与空白对照组相比,t=0.330、0.004、0.515、0.866、0.703、0.567,P>0.05;b表示与空白对照组相比,t=0.079、0.000、0.202、0.716、0.208、0.166,P>0.05;c表示与空白对照组相比,t=0.028、0.955、0.971、0.989、0.204、0.189,P>0.05。 表 3 尼可胺各剂量组雄性Wistar大鼠精子数、精子活率及精子活力的检查结果
(x±s) 组别 大鼠数量 精子数(×103个/μl) 精子活率(%) 精子活力(%) Ⅰ级 Ⅱ级 Ⅲ级 Ⅳ级 高剂量组 25 4.3±0.6a 73.4±7.5a 4.6±2.2a 20.6±6.9a 39.4±7.2a 35.4±6.7a 中剂量组 25 4.5±0.5h 72.9±7.9b 6.5±1.8h 21.8±8.6b 33.5±9.4b 38.2±12.3b 低剂量组 25 4.2±0.5c 74.3±9.3c 5.3±2.5c 24.2±10.4c 35.6±8.5c 34.9±11.8c 空白对照组 25 4.4±0.5 73.0±12.0 5.6±3.3 26.5±10.8 34.2±10.2 34.0±16.3 注:表中,a表示与空白对照组相比,t=0.618、0.878、0.325、0.028、0.043、0.615,P>0.05;b表示与空白对照组相比,t=0.471、0.967、0.147、0.097、0.824、0.537,P>0.05;c表示与空白对照组相比,t=0.200、0.679、0.941、0.465、0.599、0.753,P>0.05。 表 4 雄性Wistar大鼠尾静脉注射不同剂量的尼可胺后的脏器系数
[(x±s)%] 组别 大鼠数量 睾丸 附睾 高剂量组 25 0.86±0.12a 0.30±0.05a 中剂量组 25 0.88±0.12b 0.33±0.07b 低剂量组 25 0.87±0.14c 0.30±0.06c 空白对照组 25 0.84±0.15 0.29±0.05 注:表中,a表示与空白对照组相比,t=0.685、0.557,P>0.05;b表示与空白对照组相比,t= 0.379、0.489,P>0.05;c表示与空白对照组相比,t=0.489、0.477,P>0.05。 表 5 雄性Wistar大鼠尾静脉注射不同剂量尼可胺后的生殖毒性实验交配率
组别 交配动物数 交配成功数 交配率(%) 高剂量组 25 20 80.0 中剂量组 25 21 84.0 低剂量组 25 20 83.3 空白对照组 25 21 87.5 -
[1] Fenton BM, Lord EM, Paoni SF. Enhancement of tumor perfusion and oxygenation by carbogen and nicotinamide during single- and multifraction irradiation. Radiat Res, 2000, 153(1): 75-83. doi: 10.1667/0033-7587(2000)153[0075:EOTPAO]2.0.CO;2 [2] 顾菲, 刘晓秋, 韩英, 等.肿瘤放疗增敏药9401号的细胞毒性和体外放射增敏作用.中国辐射卫生, 2006, 15(4): 392-393. doi: 10.3969/j.issn.1004-714X.2006.04.004
[3] 刘晓秋, 王荣先, 李美佳.放射增效剂9402号对小鼠小肠隐窝上皮细胞增敏作用的研究.中国辐射卫生, 2007, 16(1): 10-11. doi: 10.3969/j.issn.1004-714X.2007.01.005
[4] Huynh PN, Hikim AP, Wang C, et al. Long-term effects of triptolide on spermatogenesis, epididymal sperm function, and fertility in male rats. J Androl, 2000, 21(5): 689-699. [5] Hikim AP, Lue YH, Wang C, et al. Posttesticular antifertility action of triptolide in the male rat: evidence for severe impairment of cauda epididymal sperm ultrastructure. J Androl, 2000, 21(3): 431-437. [6] 应俊, 姚德鸿, 尤建清, 等.精浆中催乳素浓度对精子活动力的影响.生殖与避孕, 1998, 18(3): 183-184.
[7] 胡利民, 姜民, 凌霜, 等.天然冰片与合成冰片对小鼠的一般生殖毒性.毒理学杂志, 2006, 20(4): 275-276. doi: 10.3969/j.issn.1002-3127.2006.04.030
[8] 陈波, 王汉蓉, 刘玉清, 等.风湿平胶囊对大鼠生殖功能及胚胎发育的影响.成都中医药大学学报, 2007, 30(1): 35-38. doi: 10.3969/j.issn.1004-0668.2007.01.015
[9] 人用药物注册技术要求国际协调会指导委员会.药品注册的国际技术要求(安全性部分).周海均, 译.北京: 人民卫生出版社, 2007: 87-120.
[10] 《药物生殖毒性研究技术指导原则》课题研究组. [ZH]GPT1-1药物生殖毒性研究技术指导原则.北京: 国家食品药品监督管理局, 2006.
[11] 楚宁宁, 薛青光, 孙旺吾, 等. P450芳香化酶活性调控对小鼠睾丸和附睾发育及精子发生的影响.安徽农业科学, 2009, 37(29): 14204-14206.
-





 下载:
下载: