-
胃癌术后复发是造成患者术后生存率低的主要原因之一, 即使作了根治性手术, 术后仍有30%~80%的患者会出现局部或远处复发[1]。胃癌术后的复查主要依赖X线钡餐造影和胃镜检查, 目前, 胃镜+组织活检是临床诊断胃癌术后复发最常用、最基本的方法。但是, 胃癌复发多为网膜复发、血行转移和复合复发[2], 上述检查方法的诊断价值有限, 无法为术前准确判断肿瘤浸润深度、范围以及是否有淋巴结和腹腔内脏器转移等提供足够的诊断依据。近年来, 随着MRI软硬件技术的不断发展, 特别是一些快速、超快速序列的发明与应用, 使MRI在胃肠道疾病诊断中的应用越来越广泛, 为胃癌影像学研究开辟了崭新的领域。本研究着重探讨MRI在胃癌术后吻合口复发诊断中的应用价值及临床意义。
-
选取2005年2月至2010年10月来我院就诊的43例胃癌术后患者, 他们均接受了MR、CT、X线钡餐、胃镜活检等检查。其中, 对照组为胃癌术后1~2年无复发的患者10例(男性5例、女性5例), 年龄35~76岁, 平均年龄57岁; 胃癌术后复发组33例(男性19例、女性14例), 年龄37~71岁, 平均年龄51岁, 其中, 上腹部饱胀不适者21例, 剑突下疼痛者16例, 消化道梗阻、呕吐者9例, 无症状常规检查者6例。
-
采用美国通用电气公司的GESingna Excite1.5 T高场MRI机, 配合使用体部8通道相控阵线圈。常规扫描层厚为5~8 mm, 层间隔1~2 mm, 使用30 ml动态增强造影剂欧乃影(钆双胺注射液, 上海通用电气药业有限公司生产), 注射速率为3 ml/s, 三期动态增强及延迟时间分别为15 s、30 s、60 s、3~5 min。
MR常规扫描序列: ①快速恢复快速自旋回波序列T2加权成像加呼吸门控技术, 该序列主要用于显示病变部位[5]; ②快速扰相梯度回波序列T1加权成像, 该序列主要用于观察解剖结构[5]; ③快速恢复快速自旋回波序列T2加权成像和快速扰相梯度回波序列T1加权成像加脂肪抑制技术, 可减少移动伪影和化学位移伪影的干扰, 对明确病变的组织特性和范围具有一定价值[6]; ④真稳态进动快速序列, 该序列主要用于制造液体和软组织之间的对比, 对残胃胃腔的显示效果非常好; ⑤单次激发自旋回波-回波平面成像T2加权, 该序列成像速度极快, 特别适用于临床状况较差或不能配合检查的患者, 在该序列的基础上施加扩散敏感梯度场, 即可进行水分子扩散加权成像。近年来, 扩散加权成像序列在腹部检查中的应用越来越受到重视, 为腹内脏器病变的鉴别诊断开辟了崭新的领域; ⑥MR水成像, 使含液器官的液腔突出显影, 仿真残胃胃腔, 达到或接近X线钡餐造影或胃镜的效果; ⑦快速扰相梯度回波序列T1加权动态增强扫描加脂肪抑制技术, 该序列主要用于动态增强扫描, 增强早期图像, 易于病灶的检出, 延迟扫描有助于判断残胃病变的范围及其浸润深度, 综合T1加权像和T2加权像则更有利于残胃复发灶的诊断与分期。
-
常规禁食4~8 h, 检查前10 min肌肉注射20 mg胃肠道松弛剂——山莨菪硷(654-2, 杭州民生药业有限公司生产, 青光眼及前列腺肥大患者禁用), 以松弛胃肠道平滑肌, 使其处于舒张状态, 可明显减少因胃肠道蠕动造成的运动伪影。同时, 让患者口服500~800 ml温水(MR阴性对比剂)。由于胃癌切除术后幽门括约肌功能丧失, 站立时排空较快, 故上检查床后, 使患者仰卧, 用吸管继续服200~300 ml温水, 使残胃呈中等度扩张, 有利于胃壁的良好显示, 避免了因胃壁收缩造成胃壁增厚的假象。患者体位一般取仰卧位, 也可依据病变部位的不同采用相应体位, 以使病灶与口服水接触, 形成良好对比。例如: 疑似胃前壁病变者应采用俯卧位, 行常规轴位、冠状位扫描, 以病变最大层面作为定位像, 并沿胃长轴作斜矢状位扫描[3-4]。扫描范围从膈顶到脐部, 贲门癌术后残胃的扫描范围应适当上提。
-
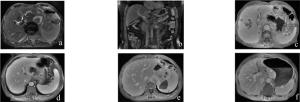
在残胃适度充盈, 使用低张剂的情况下, 胃窦、胃体、胃底的胃壁均匀一致, 厚度为(4.5±0.3)mm, 内外缘均较光滑, 内壁有时可见浅锯齿状的黏膜褶皱像。吻合口胃壁较邻近正常胃壁增厚, 厚度为(6.3±1.4)mm, 并由近胃侧向小肠侧逐渐增厚, 吻合口胃壁外缘较光整, 内缘由于手术缝合而不光整, 局部皱褶、突起(图 1)。
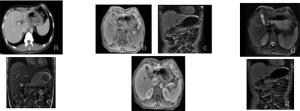
图 1 正常残胃MRI图 图中,1a:CT增强扫描示吻合口内外壁光滑,吻合口见金属银夹影;1b~1c:MR T1 加权像示吻合口外壁光整,内壁稍毛糙,壁厚度 < 8 mm;1d~1e:MR T2加权像示残胃充盈良好,吻合口通畅;1f~1g:MR增强扫描示吻合口壁粘膜层强化连续、均匀,未见明显中断。
残胃胃壁结构在快速扰相梯度回波序列T1加权像上可以辨认2~3层, 内层为较高信号, 中间层为低信号, 外层为中等信号(图 1b~1c); 快速恢复快速自旋回波序列T2加权像上胃壁内外层为高信号, 中间层为低信号, 内外层厚度较恒定, 中间层随胃膨胀的程度不同而变化(图 1d~1e)。MRI所显示胃壁的3层结构分别对应于胃壁的粘膜及粘膜下层、肌层和浆膜层。快速扰相梯度回波序列T1动态增强扫描结果显示, 胃壁粘膜及粘膜下层明显强化, 且持续时间较长(峰值时间 > 90 s), 肌层和浆膜层轻度强化, 残胃吻合口强化方式与正常胃壁一致(图 1f~1g)。
-
胃癌术后复发组33例患者中, MRI诊出30例, 其中, 残胃腔变形、狭窄者11例(图 2a); 残胃吻合口胃壁增厚 > 8 mm者30例, 吻合口邻近胃壁厚度 > 5 mm者19例, 分为局限性(图 2b)和弥漫性(图 2c)两类; 吻合口软组织肿块并邻近胃壁增厚者11例(图 2d); 肝、脾、胰腺等周围脏器浸润转移者5例(图 2c、2e); 肝胃之间、腹腔、腹膜后淋巴结转移者9例(图 2f); 增强扫描显示, 胃癌术后复发灶在动脉期不规则强化者9例, 多数病灶强化不明显, 门脉期呈渐进性强化者30例, 平衡期多数延迟强化(图 2b~2e)。
-
MRI具有良好的软组织对比度、无放射线损伤、多平面和多参数成像等优点, 能够较好地显示复发肿瘤浸润胃壁的深度、范围及病灶与周围解剖结构的关系, 还能较好地显示软组织肿块以及它们侵犯胰腺、肝脏血行转移、网膜转移以及肿大淋巴结等。其不足之处是在观察胃壁的柔软度和粘膜纠集方面有一定的局限, 对小的种植灶显示不佳。
胃癌术后残胃MRI前的准备工作非常重要, 直接关系到成像的质量[7]。残胃胃壁厚度与胃充盈、扩张程度密切相关, 不同部位的胃壁厚度也不一致。研究结果显示, 在残胃适度充盈、使用低张剂的情况下, 胃窦、胃体、胃底的胃壁均匀一致, 正常厚度不超过5 mm, > 5 mm则视为异常[8]; 残胃吻合口局部胃壁较正常明显增厚, 厚度为5~8 mm, 平均(6.5±1.6)mm。残胃吻合口的良好显示是诊断胃癌术后复发的关键。影响吻合口观察的主要因素包括吻合口的金属伪影、水肿、梗阻及残胃扩张不良造成的假性胃壁增厚等[9]。
胃癌术后复发MRI的主要表现为残胃形态改变(包括胃壁增厚、局部肿块或二者兼有[3-4, 9-10])、浆膜外侵犯和周围实质脏器、淋巴结的转移。具体表现为以下几个方面: ①吻合口复发癌常引起残胃腔变形和狭窄; ②胃壁增厚, 增厚的胃壁同时伴有信号异常, T1加权像呈等信号或稍低信号, T2加权像呈高信号或稍高信号, 多回波中随回波时间延长, 信号逐渐衰减。增强扫描结果显示, 部分胃癌复发灶在动脉期不规则强化, 多数病灶强化不明显, 门脉期呈渐进性强化, 平衡期多数延迟强化, 而未复发残胃胃壁无渐进性强化的特点。强化的范围显示了肿瘤的大小和浸润范围。门脉期和延迟期相结合, 对残胃癌的检出和定性具有重要价值[9]; ③胃壁破坏, MRI可显示胃壁低信号带的中断或明显强化, 肿瘤样病灶侵及整个胃壁; ④软组织肿块, 残胃癌向腔内或者腔外生长, 穿破胃壁与邻近肿大淋巴结融合成软组织团块, 常伴有邻近胃壁不规则增厚, 肿块的信号特征与胃壁增厚大致相仿。如肿块形成溃疡时, 可见局限性不规则的低信号或者表现为增厚胃壁上的裂隙状凹陷, T2加权像可见凹陷中充填液体的高信号龛影, 高低不等、大小不一; ⑤进展期的残胃癌常突破浆膜层侵及邻近组织器官(包括肝脏、胰腺、胆囊、十二指肠、横结肠、脾门区、腹膜、肠系膜等), 表现为病变区残胃轮廓不清、浆膜面毛糙, 可出现伸向胃周脏器的不规则条带状软组织影, 脂肪层模糊或消失, 严重的与受侵器官融合在一起, 受侵组织器官的信号改变与原发灶一致。动态增强MRI有助于鉴别肝、胰实质脏器的浸润边界; ⑥淋巴结转移多累及贲门旁、胃大小弯及幽门上下等胃壁旁浅组和脾门、脾动脉、肝总动脉及胃左动脉附近的深组等, 可以表现为淋巴结肿大超过1 cm, 并可相互融合, 也可表现为多个不足1 cm的淋巴结相互聚拢或成串排列。肿大淋巴结在T1加权像略低于肌肉信号, T2加权像亦呈稍低信号, 增强后淋巴结仅轻度强化; ⑦MRI对残胃癌转移的诊断具有较高的准确性, 胃癌以种植方式转移到网膜、肠系膜、盆腔, 表现为腹水和肿块。网膜、肠系膜显著增厚, 呈饼状或巨块状, 远处转移以肝脏、脾脏、肾上腺最常见[11]; ⑧胃癌术后残留, 术后MRI显示胃的大体解剖形态、肿瘤组织依然如初, 或者仅部分切除、造瘘等。
综上所述, MRI较好地显示了残胃壁及吻合口胃壁的厚度, 能够准确判断肿瘤浸润深度、范围、是否与周围组织有毗邻关系以及是否有淋巴结和腹腔内脏器转移等, 对指导临床手术方案的选择或综合治疗、提高胃癌术后生存率具有重要的临床意义。
高场强MRI在胃癌术后复发诊断中的应用价值
Application of high-field-strength magnetic resonance imaging to diagnose recurrent gastric carcinoma
-
摘要:
目的 探讨高场强MRI在胃癌术后复发诊断中的应用价值及临床意义。 方法 选择胃癌术后患者43例。其中,胃癌术后复发组33例,均经过消化道钡餐、CT、手术或胃镜活检和病理检查确诊;对照组10例,均经胃镜活检及病理检查证实无复发。MRI检查前使用低张剂,服用水做为阴性对比剂,应用1.5 T MR快速扰相梯度回波序列、快速恢复自旋回波序列、扩散加权成像、真稳态进动快速序列等及动态增强扫描检查方法。 结果 MRI诊出胃癌术后复发患者30例。对照组残胃壁厚度(4.5±0.3)mm,吻合口胃壁厚度(6.3±1.4)mm;复发组残胃吻合口胃壁增厚 > 8 mm者30例,吻合口邻近胃壁厚度 > 5 mm者19例,吻合口软组织肿块并邻近胃壁增厚者11例,肝脾胰腺等周围脏器转移者5例,肝胃之间、腹腔、腹膜后淋巴结转移者9例,病灶在动脉期不均匀强化者9例,静脉期及平衡期病灶呈渐进性、延迟强化者30例。 结论 MRI较好地显示了残胃壁及吻合口胃壁的厚度,能够准确判断肿瘤浸润深度、是否与周围组织有毗邻关系以及是否有淋巴结和腹腔内脏器转移等,可以用来指导临床手术方案的选择或综合治疗,对提高胃癌术后生存率具有重要的临床意义。 Abstract:Objective To evaluate the clinical application of high-field-strength magnetic resonance imaging to diagnose recurrent gastric cancer. Methods Forty three postoperative patients with gastric carcinomawere divided into two groups.The group with recurrent gastric carcinoma has 33 patients, they were clinically confirmed by barium meal of alimentary canal, CT or pathological results.There were 10 cases in control group confirmed by pathological results.All the subjects took hypotonicity agent, followed by water as negative contrastmedium.Thenpatients underwent magnetic resonance imaging including fast spoiled gradient recalled T1WI, T2WI, diffusion weighted imaging, fast imaging employing steady state sequence, magnetic resonance cholangiopancreatographyand dynamic contrast enhancement sequences when gastrointestinal tract was in hypotonic, patients drank or were primed with water as contrast. Results Thirty patients were diagnosed as recurrent gastric cancer with MRI, 28 of them were confirmed by clinical results.Three patients were missed and two patients were incorrectly misdiagnosed by MRI.Wall thickness of gastric remnant was(4.5±0.3)mm and that of stomas was(6.3±1.4)mm in control group.Types of lesions were found on MRI: thick-ening of remnant stomach stomas was more than 8 mm(n=30), thickening of neighbor rem-nant stomach stomas was more than 5mm(n=19), mass of stomas(n=11), metastasis of neighbor viscus(n=5), and metastasis of lymph nodes (n=9).On enhancement scan, 9 patients showed inhomogeneous enhancement in arterial phase and 30 patients showed gradual delayed enhancement in venous phase and equilibrium phase. Conclusion MRI is an effective imaging method in illustrating wall thickness of gastric remnant and stomas, invasion depth by carcinoma, relationship with neighbor tissue structures and metastasis of lymph nodes and abdominal viscus.It plays an important role in directing clinical therapy. -
-
[1] 胡晔, 陈炯. 复发性胃癌56例的外科治疗. 中国临床保健杂志, 2005, 8(6): 516-517. doi: 10.3969/j.issn.1672-6790.2005.06.017
[2] 刘强, 王舒宝. 复发胃癌及残胃癌的外科治疗. 中国实用外科杂志, 1998, 18(3): 494-495.
[3] 程骏, 温新东, 黎金林, 等. 进展期胃癌术前磁共振成像的研究. 温州医学院学报, 2003, 33(2): 100-101.
[4] Kang BC, Kim JH, Kim KW, et al. Value of the dynamic and delayed MR sequence with Gd-DTPA in the T-staging of stomach cancer: correlation with the histopathology. Abdom Imaging, 2000, 25(1): 14-24. doi: 10.1007/s002619910003 [5] Kato M, Saji S, Kanematsu M, et al. Detection of lymph-node metastases in patients with gastric carcinoma: comparison of three MR imaging pulse sequences. Abdom Imaging. 2000, 25(1): 25-29. doi: 10.1007/s002619910004 [6] Faber SC, Stehling MK, Holzknecht N, et al. Pathologic conditions in the small bowel: Findings at fat suppressed Gadoliniumenhanced MR imaging with an optimized suspension of oral magnetic particles. Radiology, 1997, 205(1): 278-282. doi: 10.1148/radiology.205.1.9315000 [7] 方常练. CT在胃癌检查中的价值. 江西医药, 2005, 40(11): 749-750. doi: 10.3969/j.issn.1006-2238.2005.11.038
[8] 彭卫军, 周康荣, 沈继章. 正常胃CT应用解剖和表现. 临床放射学杂志, 1997, 16(6): 348-351.
[9] 彭卫军, 周康荣, 秦新裕. CT在胃癌局部复发诊断中的应用评价. 中国癌症杂志, 2003, 13(6): 540-542. doi: 10.3969/j.issn.1007-3639.2003.06.013
[10] 倪国汉. 低场强MRI在胃癌诊断中的作用. 放射学实践, 2002, 17(2): 143-144.
[11] 谢德宁, 商秀林. 胃癌浸润转移的螺旋CT诊断. 中国误诊学杂志, 2006, 6(6): 1063-1064.
-





 下载:
下载: