-
近十多年来, 甲状腺癌发病率不断增长, 其中约90%为分化型甲状腺癌(differentiated thyroid carcinoma, DTC)[1-4]。经全甲状腺切除术后, 131I治疗和甲状腺激素抑制治疗是DTC治疗的规范模式, 而131I治疗通常在手术切除甲状腺残留组织后进行。由于131I放出γ射线能量高, 半衰期相对于其他常用核素较长、应用频率较高, 因此, 131I活度已成为核医学科中辐射防护最受关注的一类核素[5], 并且患者体内残留的131I活度已成为很多国家判定患者出院的一个标准[6]。然而, 患者体内残留131I的活度难以直接检测得到, 因此, 有必要探讨合适的体内残留活度估算方法。
131I治疗后, 摄入体内的131I大部分通过尿液在初始数日内排出[5, 7], 因此测定尿液的放射性活度不仅可以知道放射性废物的排泄信息, 同时也可了解患者体内残留活度信息。目前, 国际放射防护委员会(international commission on radiological protection, ICRP)推荐的日尿活度排泄分数值是建立在正常甲状腺基础上的[8-9], 而正常甲状腺与DTC患者甲状腺病理学是有差别的。本研究的目的是建立甲状腺切除术后经131I治疗的DTC患者尿液活度的估算模式, 该模式基于ICRP提出的放射性碘动力学模型[10], 优化了DTC患者131I治疗后尿液排泄活度的估算方法; 同时, 为验证理论估算的准确性, 对20例患者日尿活度进行了检测。结果表明, 该模式计算的日尿排泄活度分数与实验检测值能较好地吻合, 有助于DTC患者体内残留活度的估算。
-
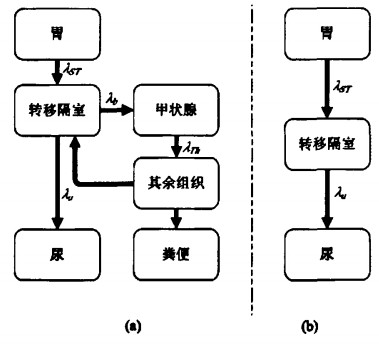
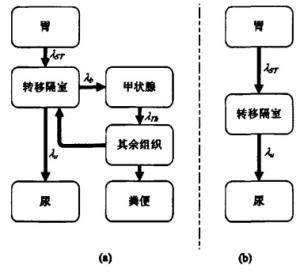
ICRP提出了131I在正常人体内代谢动力学模型, 该模型包括了图 1-a所示的几个隔室[8-10]。对于服用131I治疗的DTC患者, 在核素治疗前均经过甲状腺全切或接近全切术, 因而对于DTC患者, 其甲状腺的摄碘率可忽略不计。因此, 我们针对甲状腺手术切除后的DTC患者提出了其体内131I生物代谢模型(图 1-b)。
优化后的模型各个隔室的活度变化可表示为:
$ \frac{d q_{S T}}{d t}=\lambda_{S T} q_{S T}-\lambda_{R} q_{S T} $ $ \frac{d q_{B}}{d t}=\lambda_{S T} q_{S T}-\lambda_{U} q_{B}-\lambda_{R} q_{B} $ $ \frac{d q_{U}}{d t}=\lambda_{U} q_{B}-\lambda_{R} q_{U} $ 式中, qST、qB和qU分别为胃、转移隔室和尿液中核素的相应活度; λST为核素在胃中的廓清速度, λU为核素从转移隔室到尿液的转移速率, λR为131I物理衰变常数; 假定初始时刻(t=0)时, 胃内活度等于初始摄入活度(qi), 则尿液活度可表示为:
$ q_{U}(t)=q_{i} \frac{\lambda_{U}}{\lambda_{U}-\lambda_{S T}} e^{-\left(\lambda_{S T}+\lambda_{R}\right)^{\prime}}-q_{i} \frac{\lambda_{S T}}{\lambda_{U}-\lambda_{S T}} e^{-\left(\lambda_{U}+\lambda_{R}\right)^{\prime}} $ 在服药后第tj日, 日尿累积活度qu(tj)则可进一步推导为:
将ICRP[10]推荐的相关参数代入式(5), 可推导出日尿摄入排泄分数(intake excretion fractions, IEF(tj)):
$ \begin{gathered} IEF\left(t_{j}\right)=-2.23 \times 10^{-3}\left(e^{-24.09_{{\rm{t}}_{j - 1}}}-e^{-24.09_{{{\rm{t}}_j}}}\right)- \\ 7.6 \times 10^{-1}\left(e^{-1.324_{{\rm{t}}_j}}-e^{-1.324_{{\rm{t}}_{j - 1}}}\right) \end{gathered} $ 相比于尿液来说, 其他排泄方式可以忽略。因此服药后第tj日患者体内残留活度可粗略估计为:
$ q_{r e s}\left(t_{j}\right)=q_{i} e^{-\lambda_{R} t_{j}}\left(1-\sum\limits_{j=0}^{j} I E F\left(t_{j}\right)\right) $ -
20例DTC患者于2009年3月至2009年7月间在复旦大学附属中山医院核医学科接受131I治疗(所用131I药物由上海欣科医药有限公司生产), 治疗前均做过甲状腺切除手术, 住院时间7~10 d不等。为比较131I治疗次数是否对患者日尿活度排泄分数造成影响, 按131I治疗次数对患者进行分类, 患者年龄及给药活度等信息见表 1。
年龄(岁) 病例数* 给药活度(GBq) ≤20 1(1, 0) 3.89 20~30 3(3, 0) 3.83±0.08 30~40 6(3, 3) 3.89 40~50 8(4, 4) 3.85±0.07 50~60 1(1, 0) 3.89 60~70 1(0, 1) 5.55 ≤70 20(12, 8) 3.96±0.38 *:括号内数据前者表示首次131I治疗例数,后者表示2次以上131I治疗例数。 表 1 131I治疗分化型甲状腺癌患者年龄和给药信息
-
给予131I后以24 h为单位收集尿样, 每次采样均记录24 h尿液总体积, 采样前搅拌尿液使其活度分布均匀, 每次采样4~5 ml, 直至患者出院。
-
尿液活度的测量采用SN-695型γ活度计数仪(上海核所日环光电仪器有限公司生产), γ活度计数仪经过上海计量测试技术研究院次级标准剂量学实验室校准。测量时, 用滴定管吸取100μl尿样置于测量瓶进行检测, 每次检测3瓶, 取检测均值为实验值。给予131I后初始3 d, 由于尿液浓度过大, 超过γ活度计数仪的探测上限, 因此, 初始3 d的尿样在检测前均经过10倍的稀释。
-
对131I治疗DTC用优化模型计算和实验测量的日均尿排泄放射性活度分数值及正常人计算值见表 2。由表 2可知, DTC患者体内的大部分核素在131I治疗后初始3 d, 总摄入活度的77.9%(由优化模型计算)和78.0%(由实验检测)经尿液排出。由表 2还可看出, 采用优化模型估算DTC患者服药后第1日尿排泄131I活度分数为58.2%, 服药后初始5 d总尿排泄131I活度分数为79.3%;用γ计数仪实际检测DTC患者服药后第1日尿排泄131I活度分数均值为57.9%, 服药后初始5 d总尿排泄131I活度分数均值为79.9%。甲状腺切除手术后DTC患者与正常人日尿排泄分数比较, 前者日尿排泄活度分数值在服药后第2日开始明显大于后者。
服药后时间(d) 1 2 3 4 5 6 优化模型计算值 58.2 15.5 4.1 1.1 0.3 0.08 实验测量值 56.7±4.6 16.8±4.4 4.5±1.4 1.3±1.2 0.6±0.5 0.3±0.2 正常人计算值 (50.5~65.1) (10.0~26.7) (2.0~6.7) (0.3~5.3) (0.05~1.8) (0.02~1.2) 57.9 3.8 0.23 0.03 0.02 0.03 注: 正常人计算值参照参考文献[11]。 表 2 131I治疗分化型甲状腺癌患者与正常人日尿排泄核素放射性活度分数比较(
% ) -
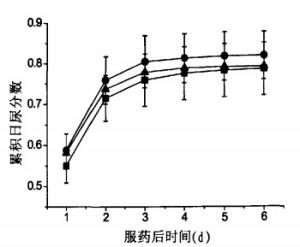
经过2次以上131I治疗的DTC患者总尿液活度排泄分数均值与首次131I治疗的患者相比略高(图 2)。
-
优化模型计算与实验检测结果表明, 经131I治疗的DTC患者体内的大部分核素在服药后初始3 d通过尿液排出, 因此在对131I治疗DTC的放射性废物管理时, 可主要考虑初始3 d的废物处理。正常人参考模型在服药后6 d内总尿液活度分数与优化模型计算值及实际检测值有明显差异, 因此在日尿排泄131I活度分数计算时, 应考虑DTC患者与正常人的差异。
采用正常人131I隔室转移参数λST和λU计算DTC患者模型日尿排泄活度分数值, 与实验检测值有较好的吻合, 表明正常人转移参数可用于甲状腺切除术后的DTC患者日尿排泄131I活度分数的计算。
实验显示, 首次131I治疗的DTC患者总尿液排泄活度分数均值低于2次以上131I治疗患者相应值, 其原因可能是多次131I治疗使患者甲状腺消除更彻底, 体内摄取131I的组织减少, 摄碘率降低, 从而使得排泄分数增加。因此, 在对实际131I治疗的DTC患者管理时, 可依据131I治疗次数对患者住院时间进行调整。但是治疗次数对于尿液排泄131I活度分数的确定性影响, 需要更多样本来确定, 治疗次数对DTC患者疗效及剂量影响也需进一步研究。
本研究推导了粗略估算DTC患者体内残留活度的计算公式, 有助于指导医院确定经131I治疗的DTC患者的出院时间, 可满足辐射防护剂量学的评价需要。若从评价患者剂量学角度出发, 仍需进一步研究体内残留活度分布及其变化。
分化型甲状腺癌患者日尿排泄131I活度分数估算
Estimation the daily urinary excretion 131I radioactivity of patients with differentiated thyroid carcinoma
-
摘要:
目的 探讨甲状腺切除术后经131I治疗的分化型甲状腺癌(DTC)患者日尿排泄131I活度分数的估算方法。 方法 建立优化隔室模型,并计算甲状腺癌患者日尿排泄131I活度分数,对20例经甲状腺切除术后的DTC患者日尿排泄131I累积活度进行检测,以验证该模型计算结果。 结果 采用优化模型估算DTC患者服药后第1日尿排泄131I活度分数为58.2%,服药后初始5 d总尿排泄131I活度分数为79.3%;用γ计数仪实际检测DTC患者服药后第1日尿排泄131I活度分数均值为57.9%,服药后初始5 d总尿排泄131I活度分数均值为79.9%。 结论 优化的DTC患者隔室模型计算日尿排泄131I活度分数简单方便,估算的日尿排泄131I活度分数值与实际检测结果吻合较好。该模型可用于估算经甲状腺切除术后的甲状腺癌患者日尿排泄131I活度分数,有助于放射性废物管理以及患者周围人员防护。 Abstract:Objective To study the methodology for calculating daily urine intake excretion fraction of 131Iin differentiated thyroid carcinoma(DTC)patients underwent thyroidectomy. Methods Simplified the current 131I compartment model with a normal thyroid.A new model was developed for calculating 131I activity excreted by urine of DTC patients.To verifiy the new method, 20 DTC patients treated with 131I therapy after thyroidectomy were investigated by measuring their daily urinary radioactivities of 131I during isolation period in this study. Results Daily urine intake excretion fractions were estimated to be 58.2%and 79.3%for the first day and 5 d respectively; the mean value for intake excretion fractions in the 20 DTC patients were 57.9% and 79.9%for the first day and 5 d respectively. Conclusions In good agreement with experimental results, the new method developed in this study was applicable to estimate the urine radioactivity intake excretion fractions of DTC patients underwent thyroidectomy.With the knowledge of daily urine intake excretion fractions, the isolation and urine storage time of DTC patients can be confirmed. -
Key words:
- Thyroid neoplasms /
- Iodine radioisotopes /
- Radiation monitoring /
- Urine /
- Radioactivity
-
表 1 131I治疗分化型甲状腺癌患者年龄和给药信息
年龄(岁) 病例数* 给药活度(GBq) ≤20 1(1, 0) 3.89 20~30 3(3, 0) 3.83±0.08 30~40 6(3, 3) 3.89 40~50 8(4, 4) 3.85±0.07 50~60 1(1, 0) 3.89 60~70 1(0, 1) 5.55 ≤70 20(12, 8) 3.96±0.38 *:括号内数据前者表示首次131I治疗例数,后者表示2次以上131I治疗例数。 表 2 131I治疗分化型甲状腺癌患者与正常人日尿排泄核素放射性活度分数比较(
% )服药后时间(d) 1 2 3 4 5 6 优化模型计算值 58.2 15.5 4.1 1.1 0.3 0.08 实验测量值 56.7±4.6 16.8±4.4 4.5±1.4 1.3±1.2 0.6±0.5 0.3±0.2 正常人计算值 (50.5~65.1) (10.0~26.7) (2.0~6.7) (0.3~5.3) (0.05~1.8) (0.02~1.2) 57.9 3.8 0.23 0.03 0.02 0.03 注: 正常人计算值参照参考文献[11]。 -
[1] Jemal A, Siegel R, Ward E, et al. Cancer statistics, 2006. CA Cancer J Clin, 2006, 56(2): 106-130. doi: 10.3322/canjclin.56.2.106 [2] Liu S, Semenciw R, Ugnat AM, et al. Increasing thyroid cancer incidence in Canada, 1970-1996: time trends and age-period-cohorteffects. Br J Cancer, 2001, 85(9): 1335-1339. doi: 10.1054/bjoc.2001.2061 [3] Davies L, Welch HG. Increasing incidence of thyroid cancer in the United States, 1973-2002. JAMA, 2006, 295(18): 2164-2167. doi: 10.1001/jama.295.18.2164 [4] Kent WD, Hall SF, Isotalo PA, et al. Increased incidence of differentiated thyroid carcinoma and detection of subclinical disease. CMAJ, 2007, 177(11): 1357-1361. doi: 10.1503/cmaj.061730 [5] International Commission on Radiological Protection. Release of patients after therapy with unsealed radionuclides. Ann ICRP, 2004, 34(2): v-vi, 1-79. doi: 10.1016/j.icrp.2004.08.001 [6] Muhammad W, Faaruq S, Matiullah, et al. Release criteria from hospitals of 131I thyrotoxicosis therapy patients in developing countries—case study. Radiat Prot Dosimetry, 2006, 121(2): 136-139. doi: 10.1093/rpd/ncl003 [7] Driver I, Packer S. Radioactive waste discharge quantities for patients undergoing radioactive iodine therapy for thyroid carcinoma. Nucl Med Commun, 2001, 22(10): 1129-1132. doi: 10.1097/00006231-200110000-00012 [8] 方军, 董柳灿译. 工作人员的放射性核素摄入量限值. 国际放射防护委员会第30号出版物(第一部分). 北京: 原子能出版社, 1984: 152.
[9] International Commission on Radiological Protection. Age-dependent doses to members of the public from intake of radionuclides: part 1. A report of a Task Grop Committee of the International Commission on Radiological Protection. Ann ICRP, 1989, 20(2): 1-122. [10] International Commission on Radiological Protection. Individual monitoring for internal exposure of workers replacement of ICRP publication 54. Ann ICRP, 1997, 27(3-4): 1-161. doi: 10.1016/S0146-6453(98)00004-9 [11] Lessard ET, Xia YH, Skrable KW, et al. Interpretation of bioassay measurements. New York: US Nuclear Regulatory Commission, NUREG/CR-4884, 1988: B-58 -





 下载:
下载: