-
在国家职业卫生标准GBZ 97-2009《放射性肿瘤病因判断标准》实施期间,中国医学科学院放射医学研究所(简称放射所)主持研发了其计算机计算系统[1]。随后,放射所领衔修订了GBZ 97-2009,起草了GBZ 97-2017《职业性放射性肿瘤判断规范》。基于同样的出发点,放射所研发了GBZ 97-2017配套的“职业性放射性肿瘤判断规范计算机系统”[2-3](简称计算机系统)。
GBZ 97-2017中使用的外照射致癌的方法学由放射所提出,在项目组组织的专家研讨会上,得到了领域内专家的认可并采用。标准正文中的参数列表,除了有正式参考文献出处的和部分正式发表的[4-8],其余均为原创首发数据。所有方法学内容均在标准审核中以编制说明形式请同行专家审议通过。这些原创方法学及其得到的数据均采用了程序化计算的方法。受版面所限,标准文本选取了其中的主体数据。计算机系统涵盖了标准编制过程中的程序化计算及其产生的所有数据。
本解析介绍了计算机系统病因概率(probability of causation,PC)估算的方法学,以便于标准使用者理解和正确使用该标准、相关领域研究人员了解该领域的科学研究现状,并据此发现其改进空间。
-
放射性肿瘤与其他肿瘤不能通过临床和(或)实验室方法进行区分,需要探索其他方法。建立并使用PC方法判定肿瘤的放射性病因是从美国开始的[9]。放射流行病学研究成果为使用该方法进行病因判断提供了关键的基础数据。PC推导过程见以下公式[9]:
$ {{{E}}_{\text{超额}}}{\rm{ = }}{{{P}}_{\text{暴露}}}{\rm{ - }}{{{P}}_{\text{零暴露}}} $ $ {{ERR}}= {{E}}_{\text{超额}}/{{P}}_{\text{零暴露}} $ $ {{PC}}= {{E}}_{\text{超额}}/{{P}}_{\text{暴露}} $ 将公式(1)、(2)代入公式(3):
$ {{PC = }}{{{E}}_{\text{超额}}}{\rm{/}}\left( {{{{E}}_{\text{超额}}}{\rm{ + }}{{{P}}_{\text{零暴露}}}} \right){{ = ERR/}}\left( {{{ERR + 1}}} \right) $ 以上公式中,ERR为超额相对危险(excess relative risk, ERR);P暴露指在电离辐射暴露下人群的癌症发生率;P零暴露指同一人群在没有电离辐射暴露下的癌症发生率。根据公式(1),E超额为由于电离辐射原因所导致的该人群癌症发生率的绝对增加值。根据公式(2),ERR为E超额占P零暴露的百分数。根据公式(3)及推导所得的公式(4),PC为E超额占P暴露的百分数,是指P暴露中因电离辐射导致癌症发生增加绝对值占P暴露的百分数。而P暴露中PC之外的份额就是基线癌症发生所占P暴露的百分数。公式(1)~(3)均是人群暴露与其癌症发生的关系,因此据此推导所得公式(4)也是表示人群暴露与其癌症发生的关系。标准中把PC值赋予个人,其理论假设是此人是该公式中参数出处人群的典型成员。
-
基于PC相关基础研究的发展,考虑到旧版国家标准GBZ 97-2009中最亟待改进的内容,选用电离辐射生物效应委员会报告7第2部分(BEIR VII Phase 2,2006)的危险估算模型[10]。这一模型主要是基于日本原子弹爆炸幸存者的终身寿命研究(life span study,LSS)1958–1998年实体癌发病率、1950–2000年白血病死亡率和DS02剂量体系数据建立而成[10]。此外,女性乳腺癌危险模型所依据的8个队列包括4个美国人群队列;甲状腺癌危险模型所依据的6个队列包括3个美国人群队列,2个国际队列。因此,上述队列模型及其危险系数是LSS的,女性乳腺癌和甲状腺癌对美国人群有一定的代表性。
-
胃、结肠、肝、肺、膀胱、食管、骨和关节等实体癌危险模型见公式(5):
$ ERR\left( {EAR} \right) = \beta s \times D \times exp[( {\textit{ɣ}}\times e^*)] \times \left( {a/60} \right)^{ \textit{ɧ}} $ 公式(5)中,EAR为超额绝对危险,βs为性别危险系数,D为剂量(Sv),ɣ为受照年龄函数,e为受照年龄,a为患癌年龄,ɧ为患癌年龄函数。当e≥30时,e*=0;当e<30时,e*=(e-30)/10。公式(5)参数值见BEIR VII Phase 2[10]。
-
女性乳腺癌危险模型见公式(6):
$\begin{aligned} EAR/{\text{万人}}\cdot{\text{年}}\cdot Sv = & 9.9 \times exp[ - 0.05 \times \left( {e \!-\! 25} \right)] \times\\ & \left( {a/50} \right)^{ \textit{ɧ}} \end{aligned}$ 公式(6)中,EAR为超额绝对危险,e为受照年龄,a为患癌年龄,ɧ为患癌年龄函数,其取值分别为3.5(a<50岁)和1(a≥50岁)。公式(6)中9.9采用网络版[11]。网络版数据与纸质版数据不一致,网络版数据为勘误后数据。
-
甲状腺癌危险模型及参数赋值见公式(7):
$ ERR/Sv = \beta s \times exp[ - 0.083 \times \left( {e - 30} \right)] $ 公式(7)中,βs为性别危险系数,其中,男性为0.53、女性为1.05,e为受照年龄。
-
白血病危险模型见公式(8):
$\begin{aligned} ERR/EAR =& \beta s \times D \times (1 + \theta \times D) \times exp[ {\textit{ɣ}}\times \\ &e + \delta \times log(t/25) + \Phi \times e \times log(t/25)] \end{aligned}$ 公式(8)中,EAR为超额绝对危险,βs为性别危险系数,D为剂量(Sv),θ为剂量参数系数,ɣ为受照年龄系数,e为受照年龄,δ为间隔时间系数,t为间隔时间,Φ为受照年龄和间隔时间系数,是患癌年份到受照年份的间隔时间,单位为年。公式(8)参数值参见BEIR VII Phase 2[10]。
-
为了将LSS的ERR用于我国职业照射人群的肿瘤放射性病因判断,需要对其进行一系列的校正。主要包括根据LSS的ERR估算我国人群ERR,使用潜伏期校正因子调整潜伏期间照射ERR,使用剂量和剂量率效应因子(dose and dose-rate effective factor,DDREF)校正低剂量和低剂量率电离辐射的ERR和使用吸烟校正因子校正肺癌患者中吸烟因素对ERR的影响。
-
BEIR VII Phase 2是根据日本人群危险,经过人群间危险转移,估算了美国人群危险,即实现了日本人群危险的美国化。本文主要参考该方法。BEIR VII Phase 2中未提供女性乳腺癌和甲状腺癌危险转移方法。其推荐了这二者的最佳危险模型和相应危险系数分别为女性乳腺癌EAR和甲状腺癌ERR。本文即选用依据这两个系数的危险转移模型,即女性乳腺癌采用相加模型,甲状腺癌采用相乘模型。相乘模型是假定我国人群单位剂量ERR与LSS相同,相加模型是假定我国人群单位剂量EAR与LSS相同。相乘和相加混合模型是假定我国人群单位剂量ERR是相乘模型和相加模型按照一定权重组合。
在日本人群单位剂量ERR和(或)EAR基础上,经过人群间危险转移公式(9)~(12),结合我国人群肿瘤基线发病率,估算我国人群单位剂量ERR。胃、结肠、肝、膀胱、食管、骨和关节、白血病危险转移模型见公式(9)[10]:
$ ER{R_{\text{转移}}} = 0.7 \times ERR + 0.3 \times EAR/B $ 公式(9)中,ERR转移为转移后的我国的上述肿瘤ERR;ERR和EAR为根据公式(5)或公式(8)估算得到的上述癌症的LSS超额相对和绝对危险,B为我国2009年上述肿瘤男/女性年龄组别的基线发病率。
肺癌危险转移模型见公式(10)[10]:
$ ER{R_{\text{转移}}} = 0.3 \times ERR + 0.7 \times EAR/B $ 公式(10)中,ERR转移为转移后的中国肺癌ERR;ERR和EAR为根据公式(5)估算得到LSS肺癌的超额相对和绝对危险,B为我国2009年肺癌男/女性年龄组别基线发病率。
女性乳腺癌危险转移模型见公式(11):
$ ER{R_{\text{转移}}} = {\rm{ }}EAR/B $ 公式(11)中,ERR转移为转移后的中国女性乳腺癌ERR;EAR为根据公式(6)求得的LSS女性乳腺癌超额绝对危险,B为我国2009年女性乳腺癌年龄组别基线发病率。
甲状腺癌危险转移模型见公式(12):
$ ER{R_{\text{转移}}} = {\rm{ }}ERR $ 公式(12)中,ERR转移为转移后的中国甲状腺癌的ERR;ERR为根据公式(7)估算得到的LSS甲状腺癌超额相对危险。
我国各种肿瘤性别-发病年龄组别基线发病率取各肿瘤1~84岁的各年龄组发病率,包括1~4岁组,5~84岁组共16组(5岁/组)。基于最小二乘法原理,使用C++语言估算每一年的肿瘤-性别-患癌年龄组别基线发病率。当拟合发病率为负数时,认为其为0.001例/万人·年。
-
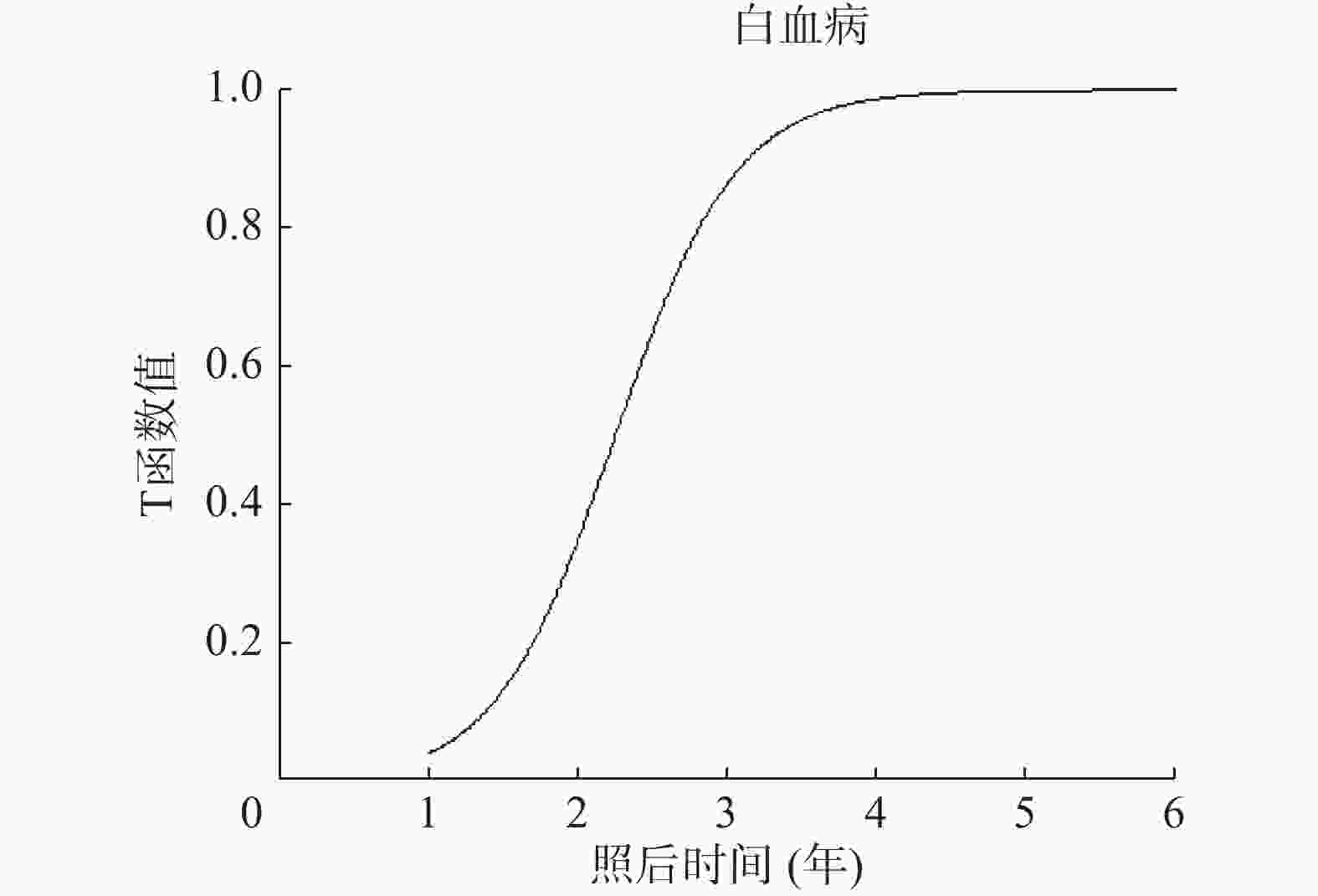
潜伏期校正函数(S型函数)见公式(13)[12]:
$ F(t) = \frac{1}{{1 + {e^{\frac{{ - (t - \mu )}}{S}}}}} $ 公式(13)中,F(t)为潜伏期函数,t为潜伏期(单位年),e为受照年龄,μ为函数中点值,s为形状参数。
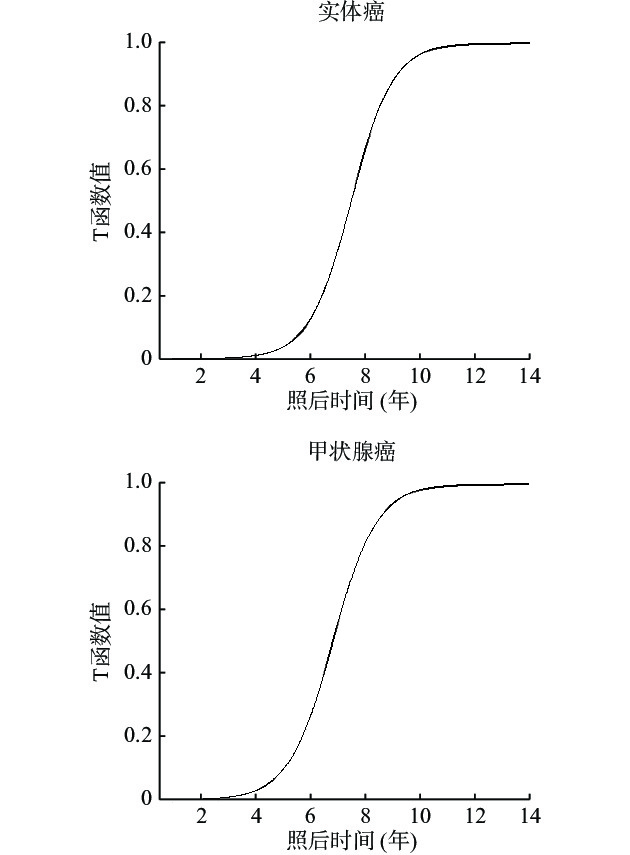
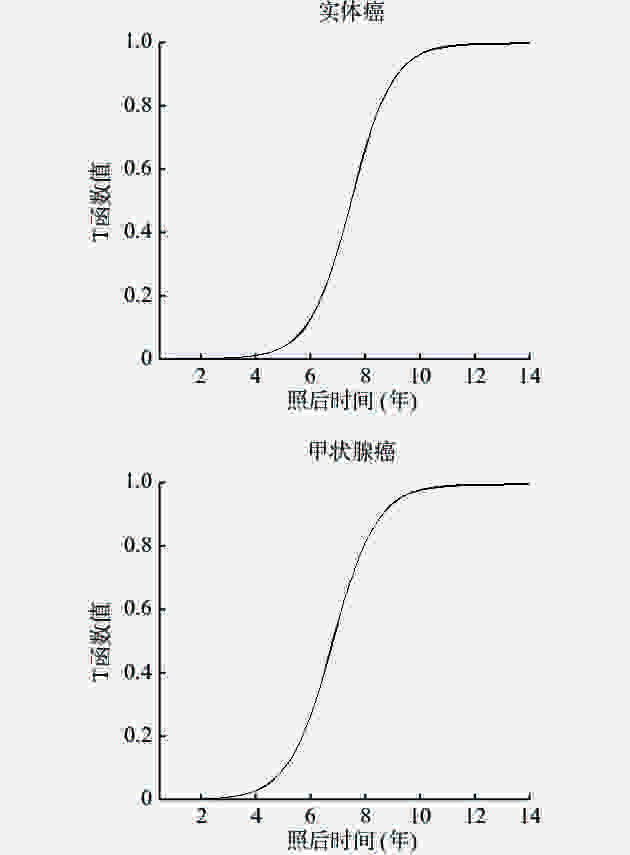
在本文中,我们假定癌症潜伏期校正因子为最大值(0.99)、最小值(0.01)和中点值时,实体癌潜伏期分别为4年、11年和7.5年;甲状腺癌潜伏期分别为2.5年、7.6年和5.05年;白血病潜伏期分别为0.4年、4.1年和2.25年。分别将3种肿瘤上述3个值代入公式(13),估算出3种肿瘤函数式的函数中点值和形状参数分别为7.5、5.05、2.25和0.76168、0.55494、0.40260。根据潜伏期函数估算3种肿瘤潜伏期内逐年的校正因子(图1~2)。
-
吸烟是肺癌的一种重要的致癌因素,辐射致癌归因分析中需要剔除吸烟因素的影响。引入吸烟校正因子的目的就是要剔除患者肺癌发生的吸烟因素的归因份额。某肺癌患者可根据其某暴露年吸烟量及其性别,使用其特有的吸烟校正因子对该年的辐射致癌危险进行校正。
本标准直接引用了美国NIH 03-5387中使用的系列的吸烟校正因子[10]。对男性和女性共9种吸烟情况分别给出了校正值。校正因子的估算需要人群队列研究估算各个吸烟量人群肺癌发生的相对危险值,还需要目标人群的吸烟分布数据,即人群中各个吸烟量人群的百分比分布。目前本标准中校正因子的基础数据为美国一战退伍军人队列研究和美国1964-1965年人群吸烟分布研究[13]。这一数据对我国职业人群代表性不好,亟待调研和整合我国人群相关数据,提高该数据对我国人群的代表性。
-
BEIR VII的危险估算模型是基于LSS队列数据的。BEIR VII研究认为该队列研究所得辐射致实体癌危险系数不能直接用于低剂量和低剂量率照射情况,需要经过DDREF校正。校正方法是用LSS的实体癌危险系数除以1.5。白血病的危险模型为线性平方式,白血病不需要经过DDREF校正。
-
GBZ 97-2017计算机系统的版面设计较GBZ 97-2009的计算机系统有优化。GBZ 97-2009的计算机系统使用的是开发系统默认的版面。而GBZ 97-2017计算机系统是由美工设计的界面,设置了系统登录界面、计算主界面和数据库管理界面,界面功能区划分清晰。
GBZ 97-2017计算机系统是基于Visual Studio 2008开发平台搭建的计算框架。建立PC计算所需数据库,通过C++程序语言实现PC计算程序化。软件还进行了计算的准确性测试:首先拟定包括所有肿瘤类型、所有计算公式和参数、所有参数表格节点数据的200例实例,然后分别进行手工计算和软件计算。对经过两种方法计算出的结果进行比较分析,软件计算准确率达100%。
-
计算机系统需要录入患者的基本信息、剂量信息以计算PC值。其中,患者基本信息包括计算用必填信息[性别、出生年份、确诊年份、肿瘤类型(食管癌、胃癌、结肠癌、肝癌、外照射致肺癌、氡致肺癌、骨和关节恶性肿瘤、女性乳腺癌、膀胱癌、甲状腺癌,除了慢性淋巴细胞白血病以外的所有类型白血病)]和选填信息(个人证件类型、证件号码)。
患者剂量信息包括受照年份、逐年的累积器官剂量(cSv)以及逐年的吸烟情况。肺癌情况下,首先勾选照射类型,氡子体照射或外照射。氡致肺癌有吸烟和不吸烟两种选项,外照射致肺癌有9种吸烟情况选项。
计算结果列出PC的均值,PC的95%可信限上限,PC的95%可信限上限校正值3项。最终判定值为PC的95%可信限上限校正值。当该值≥50%时,判定为职业性放射性肿瘤。
-
尽管GBZ 97-2017所选用的危险模型较美国现行判断方法的模型依据更新,但是这些模型均依据其他国家人群的研究数据,没有我国人群的研究数据。如女性乳腺癌模型,美国人群研究数据可以直接获得其危险模型[10]。我国没有相关的队列研究数据,需要进行人群间危险转移,根据他国的危险模型估算我国人群的危险模型。开展我国人群研究,直接获取我国人群危险模型会大大提高我国国家标准研究数据的代表性。
其次,所采用的危险转移模型及其后面的一系列校正,从方法学上均直接采用了美国方法,没有实现其中国化。如吸烟校正因子,无论是方法学上,还是基础数据,均没有我国原创数据,对我国人群适用性较差。
该系统所依据的GBZ 97-2017是以个人逐年累积器官剂量为基础的,而个人器官剂量本身需要依据另外的国家标准估算。所以使用该软件前,首先需要根据患者的具体情况,选择并依据相应的国家标准,估算该患者逐年的器官累积剂量,为该软件的使用提供录入的基础数据。
该系统为单机版软件,目标人群为专业的职业病判断医师,可以作为判断医师的辅助诊断工具。然而由于目前电离辐射技术的应用日益广泛,接受电离辐射职业照射的人群有35万[14]。我国人群的终身患癌风险达到27.8%[15],即每3~4人一生中就有约1人被诊断为癌症。一旦相关民众患癌,首先要排除其职业照射病因。为此,有职业性放射性肿瘤判断需求的人群数量不容小觑。目前,尽管能诊断为职业性放射性肿瘤的人数有限,但需要进行职业性放射性肿瘤病因判断以排除其职业因素的人数却很多。可以在公众正式申请官方的职业性放射性肿瘤病因判断之前,向其开放一个自测的网络版软件。该网络软件现已完成研发[3],目前待试用。对绝大多数公众而言,使用网络软件自测,一来可以增加其对职业照射致癌危险的一个量化认识,二来可以大大降低职业性放射性肿瘤判断官方申请的数量,减少职业病诊断医师的工作量,也会间接减少该领域社会舆情。实现与国际接轨。
-
本文主要介绍了GBZ 97-2017编制所依据的危险模型、危险转移模型及一系列校正方法。较前一版标准,GBZ 97-2017实现了辐射致癌危险系数的中国化,这一环节大大提升了该数据对我国人群的代表性。要进一步提升该标准对我国人群的适用性,亟待改进的内容包括定量各环节参数的不确定性,实现吸烟校正因子的中国化。
GBZ 97-2017是强制性国家标准,在我国根据其判断的职业性放射性肿瘤患者可以依法获得职业赔偿。GBZ 97-2017的编制,既需要考虑科学因素,又需要综合社会政策因素。尽管从科学性考虑,该标准存在诸多的不确定性,但是从判定界限值的角度,取均值的95%的可信限上限值为判定界限值来看,该标准判定门槛较低,有利于职业性放射性肿瘤患者。
利益冲突 本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明 孙志娟参与命题的提出和设计,负责文献的检索、论文的撰写、修改和定稿;刘强、涂文军、王芹、王津晗负责命题的设计和论文的修改;王彦、杜利清、徐畅负责论文的修改;王继先负责命题的提出和设计、论文的撰写和审阅。
GBZ 97-2017 《职业性放射性肿瘤判断规范》 解析——职业性放射性肿瘤判断规范计算机软件
Dissection of GBZ 97-2017 Judgment standard for occupational radiogenic neoplasms—A computer software for occupational radiogenic neoplasm judgment
-
摘要: GBZ 97-2017《职业性放射性肿瘤判断规范》领衔起草单位——中国医学科学院放射医学研究所研发了其配套的计算机软件。笔者主要介绍了该软件的计算逻辑,即GBZ 97-2017的病因概率估算的方法学,包括病因概率可进行病因判断的理论基础、辐射致癌危险模型及其中国化的人群间危险模型、使用吸烟校正因子剔除肺癌的吸烟归因份额、使用剂量和剂量率校正因子估算低剂量照射危险和使用潜伏期校正因子校正肿瘤潜伏期内照射危险,以及GBZ 97-2017配套软件研发的概况及不足之处,并建议开发网络版软件。Abstract: As the leading institute of the draft group, the Institute of Radiation Medicine, Chinese Academy of Medical Sciences drafted "Judgment standard for occupational radiogenic neoplasms" GBZ 97-2017 and developed its software. This paper introduces the calculation logic of the software, as follow: the methodology of probability of causation in GBZ 97-2017, including the theoretical basis of rationality for using causation probability for the judgment of radiogenic neoplasms; Japanese risk model in estimating cancer risks induced by ionizing radiation and risk transfer model from Japanese population to Chinese population; and use of smoking correction factors to eliminate smoking attribution to lung cancer. This paper introduces the general situation of GBZ 97-2017 software development and its deficiencies and suggests the development of an online software.
-
[1] 孙志娟, 王继先, 向剑, 等. 放射性肿瘤病因概率的计算机计算系统[J]. 辐射研究与辐射工艺学报, 2014, 32(5): 23−27. DOI: 10.11889/j.1000−3436.2014.rrj.32.050203.
Sun ZJ, Wang JX, Xiang J, et al. Computer calculating system for probability of causation of radiogenic neoplasms[J]. J Radiat Res Radiat Process, 2014, 32(5): 23−27. DOI: 10.11889/j.1000−3436.2014.rrj.32.050203.[2] 中国医学科学院放射医学研究所. 职业性放射性肿瘤判断计算机系统: 中国, 2017SR401537[P]. 2017−07−26.
Institutes of Radiation Medicine, Chinese Academy of Medical Sciences. Computer system for judgment of occupational radiation neoplasms: CN, 2017SR401537[P]. 2017−07−26.[3] 中国医学科学院放射医学研究所. 职业性放射性肿瘤判断网络软件1.0.0[P]. 中国. 2019SR0176795. 2019−2−25.
Institutes of Radiation Medicine, Chinese academy of medical sciences, Network software for judgment of occupational radiation neoplasms 1.0.0[P]. China. 2019SR0176795. 2019−2−25.[4] 陈景云, 孙志娟, 任冠华, 等. 辐射致白血病危险从日本人群向中国人群的转移探讨[J]. 中华放射医学与防护杂志, 2015, 35(2): 134-138. DOI: 10.3760/cma.j.issn.0254−5098.2015.02.014.
Chen JY, Sun ZJ, Ren GH, et al. Transfer of radiation related leukemia risk from Japanese population to Chinese population[J]. Chin J Radiol Med Prot, 2015, 35(2): 134-138. DOI: 10.3760/cma.j.issn.0254−5098.2015.02.014.[5] 孙志娟, 王继先, 孙全富, 等. 中国人群辐射致肝癌危险系数估算研究[J]. 中国职业医学, 2015, 42(6): 636−639, 644. DOI: 10.11763/j.issn.2095−2619.2015.06.008.
Sun ZJ, Wang JX, Sun QF, et al. Estimation of the risk coefficients of radiogenic liver cancer in the Chinese population[J]. China Occup Med, 2015, 42(6): 636−639, 644. DOI: 10.11763/j.issn.2095−2619.2015.06.008.[6] 孙志娟, 王继先, 向剑, 等. 我国人群辐射致肺癌危险系数估算研究[J]. 中华肿瘤防治杂志, 2015, 22(13): 993−997. DOI: 10.16073/j.cnki.cjcpt.2015.13.001.
Sun ZJ, Wang JX, Xiang J, et al. Estimation of radiogenic lung cancer risk coefficients for Chinese population[J]. Chin J Cancer Prev Treat, 2015, 22(13): 993−997. DOI: 10.16073/j.cnki.cjcpt.2015.13.001.[7] 孙志娟, 王继先, 向剑, 等. 我国人群辐射致胃癌危险系数估算研究[J]. 中华放射医学与防护杂志, 2015, 35(4): 282−286. DOI: 10.3760/cma.j.issn.0254−5098.2015.04.011.
Sun ZJ, Wang JX, Xiang J, et al. Estimation of radiogenic cancer risk coefficients of stomach cancer in Chinese population[J]. Chin J Radiol Med Prot, 2015, 35(4): 282−286. DOI: 10.3760/cma.j.issn.0254−5098.2015.04.011.[8] 孙志娟, 王继先, 孙全富, 等. 我国人群辐射致结肠癌危险系数估算[J]. 辐射防护, 2016, 36(2): 76−81.
Sun ZJ, Wang JX, Sun QF, et al. Estimation of radiogenic colon cancer risk coefficients for Chinese population[J]. Radiat Prot, 2016, 36(2): 76−81.[9] National Institutes of Health. Report of the National Institutes of Health Ad Hoc Working Group to develop radioepidemiological tables[R]. NIH Publication No. 85-2748, Washington: NIH, 1985. [10] NRC. Health risks from exposure to low levels of ionizing radiation: BEIR VII phase 2[M]. Washington, DC: The National Academics Press, 2006: 1-406. [11] NRC. Health risks from exposure to low levels of ionizing radiation: BEIR VII phase 2[EB/OL]. (2006-12-30)[2018-09-22]. https://www.nap.edu/read/11340/chapter/14#273. [12] Kocher DC, Apostoaei AI, Henshaw RW, et al. Interactive radioepidemiological program (IREP): a web-based tool for estimating probability of causation/assigned share of radiogenic cancers[J]. Health Phys, 2008, 95(1): 119−147. DOI: 10.1097/01.HP.0000291191.49583.f7. [13] 杨晴晴, 孙志娟, 赵永成. 吸烟对外照射致肺癌危险的校正因子研究[J]. 中华放射医学与防护杂志, 2015, 35(8): 638−640. DOI: 10.3760/cma.j.issn.0254−5098.2015.08.020.
Yang QQ, Sun ZJ, Zhao YC. Study on smoking-related adjustment factors for radiogenic lung cancer risk[J]. Chin J Radiol Med Prot, 2015, 35(8): 638−640. DOI: 10.3760/cma.j.issn.0254−5098.2015.08.020.[14] Sun QF. Occupational exposure in China[J]. Jpn J Health Phys, 2016, 51(2): 89−91. DOI: 10.5453/jhps.51.89. [15] 李小亮, 牛昊巍, 孙全富, 等. 我国辐射相关癌症终生危险基线值估计[J]. 中华放射医学与防护杂志, 2011, 31(6): 695−697. DOI: 10.3760/cma.j.issn.0254−5098.2011.06.019.
Li XL, Niu HW, Sun QF, et al. Estimation of baseline lifetime risk of developed cancer related to radiation exposure in China[J]. Chin J Radiol Med Prot, 2011, 31(6): 695−697. DOI: 10.3760/cma.j.issn.0254−5098.2011.06.019. -





 下载:
下载: